Константа - кислотная диссоциация
Cтраница 2
На основании сопоставления констант кислотной диссоциации можно допустить, что по суммарному влиянию на эффективный заряд центрального атома а-донорных и я-акцепторных свойств триэтилфосфит и тиоэфиры близки друг другу. По первой ступени он диссоциирует как сильная кислота, а / Сал. [16]
Гильденгершель для расчета констант кислотной диссоциации рекомендует вначале определить ориентировочное значение константы по точце на кривой титрования, соответствующей 0 5 эквивалента добавленной щелочи. [17]
Распространенным методом определения констант кислотной диссоциации является также спектрофотометрический. Для применения этого метода Необходимо, чтобы существовала область спектра, в которой молярные коэффициенты погашения кислотной и основной форм заметно различались. [18]
Первая и вторая константы кислотной диссоциации К и К. [19]
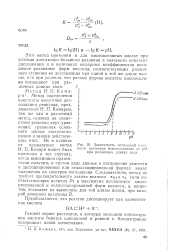 |
Зависимость оптической плотности растворов бензоилацетона от рН при различных длинах волн. [20] |
Метод определения L константы кислотной диссоциации реактива, предложенный Н. П. Комарем, так же как и расчетный метод, основан на совместном решении двух уравнений: уравнения основного закона светопогло-щения и закона действующих масс. Но в отличие от предыдущих метод Н. П. Комаря может быть применен в тех случаях, когда невозможно практически получить в чистом виде данные о поглощении реагента в диссоциированной или недиссоциированной формах ввиду наложения их спектров поглощения. [21]
Действительно, сравнение констант кислотной диссоциации изученных реагентов ( гГ) т 2 20 - 10-пи HjBm 3 28 - Ю-10) показывает, что бензоилметилдиоксим обладает более ясно выраженными кислотными свойствами, или, иными словами, водород оксимной группы последнего более подвижен, чем водород оксимной группы диметилдиоксима. Сравнительно небольшое различие констант кислотной диссоциации упомянутых реагентов объясняется относительно слабым отрицатель - ным индукционным эффектом группы СвН6 - и некоторой удаленностью последней от оксимной группы. [22]
Таким образом, константу кислотной диссоциации иона NH можно просто представить в виде [ NH3 ] [ H3O ] / [ NH4 ], где NH3 обозначает суммарную концентрацию неионизованных молекул аммиака в растворе, независимо от степени их гидратации. [23]
Величину К называют константой кислотной диссоциации. [24]
Многими авторами были определены константы кислотной диссоциации некоторых Л - аридгидрокеамовых кислот [ 23, 24, 27, 283 - Но-лученные результат увязывались о природой заместителей и характером растворителя. Например, в работе [ 27J показано, что природа заместителя влияет не только на значение рКа, но и на переход п - &. [25]
Зная kh, и константы кислотной диссоциации диаквотетр-лммин-иона, найденные Ламом и Деймоном, можно вычислить пятую ступенчатую константу устойчивости. [26]
 |
Константы кислотной диссоциации замещенных бензойных кислот в 50 % - ном этаноле при 25 С. [27] |
В табл. 39 приведены константы кислотной диссоциации фенолов, имеющих в мета - или raapa - положениях алкилсульфинильную и алкилсульфонильную группы. [28]
Зная kh, и константы кислотной диссоциации диаквотетр-аммин-иона, найденные Ламом и Деймоном, можно вычислить пятую ступенчатую константу устойчивости. [29]
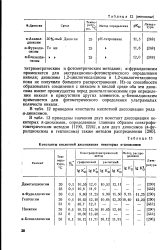 |
Константы кислотной диссоциации некоторых а-диоксимов. [30] |
Страницы: 1 2 3 4