Константа - кислотная диссоциация
Cтраница 3
В табл. 12 приведены константы кислотной диссоциации ряда а-диоксимов. [31]
В табл. 1 приведены константы кислотной диссоциации гидроксильных групп изучавшихся соединений, определенные спек-трофотометрическим методом. [32]
Определенные в настоящее время константы кислотной диссоциации некоторых алкилфенолов показывают, что численные значения рКа в воде для фенола и его м - и п-алкилфенолов составляют 9 95 - 10 23 ед. [33]
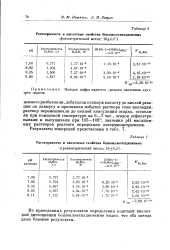 |
Растворимость и кислотные СЕОЙСТВЗ бегооилметилдиоксвма. [34] |
Из приведенных результатов определения констант кислотной диссоциации бензоилметилдиоксима видно, что оба метода дали близкие результаты. [35]
Каждый изгиб кривой соответствует определенной константе кислотной диссоциации. [36]
Здесь величина Ка называется константой кислотной диссоциации ( ионизации) или просто константой кислотности. [37]
Интересно проследить зависимость между константой кислотной диссоциации нитрофенола и интервалом рН его экстракции. [38]
Для количественного подтверждения сказанного сопоставим константы кислотной диссоциации и константы устойчивости комплексов различных N-замещенных иминодиуксусных кислот. [39]
Вессели и Лайнен [137] определили константы кислотной диссоциации 5-ацетоацетил - К - ацетилтиоэтаноламина и этилацетоацетата. [40]
 |
Константы кислотной диссоциации диаквокомплексов типа [ PdL ( H2O 2 ] 2 ( при 25 С. [41] |
Следует отметить, что вторые константы кислотной диссоциации диакводиаминных соединений, соответствующих тиоэфирным, а также триэтилфосфитного комплекса типа u uc - [ Pi L2 ( H2O) 2 ] 2 - величины одного порядка. Если связывать кислотные свойства с эффективным зарядом на центральном атоме или на лигандах ( в частности, на атоме кислорода в молекуле воды), можно сделать заключение, что в моно-гидроксильных комплексах аминного [ Pt A2 ( H2O) OH ] и тиоэфир-ного, а также фосфитного типов [ Pt Ь2 ( Н2О) ОН ] эффективные заряды практически одинаковы. Это может быть обусловлено тем, что в тио-эфирных и фосфитном комплексах неподеленная электронная пара координированной гидроксильной группы смещена к дентральному атому по я-типу. Поскольку амины ( аммиак и алифатические амины) не обладают л-акцепторными свойствами, то в данном случае гидро-ксильная группа не проявляет столь сильно я-донорные свойства. В результате различного поведения гидроксилъного лиганда в тио-эфирных и фосфитном комплексах, с одной стороны, и в аминных, с другой, происходит выравнивание эффективных зарядов на центральном атоме ( а затем на атоме кислорода координированной молекулы воды) и константы диссоциации по второй ступени становятся практически одинаковыми. [42]
В дополнительных таблицах мы приводим константы кислотной диссоциации неорганических и органических соединений в водных растворах при температуре 2 5 С. [43]
Даны также спектрофотометрические методы определения констант кислотной диссоциации органических реагентов, проявляющих слабую кислотную функцию. Все эти примеры ярко показывают преимущество спектрофотометров - приборов, имеющих высокую степень монохроматизации. [44]
 |
Константы кислотной диссоциации и значения о сульфопроизводных анилина, фенола и бензойной кислоты в 0 1 н. растворе KCI при 25 С. [45] |
Страницы: 1 2 3 4