Константа - михаэлис
Cтраница 1
Константа Михаэлиса для реакции кислорода с цитохромок-сидазой невелика. Ее можно экспериментально оценить, исследуя дыхательную активность изолированных митохондрий при различных концентрациях кислорода. [1]
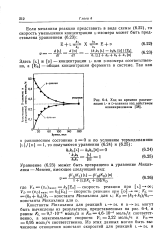 |
Ход во времени рацемизации L - и D-аланина под действием аланинрацемазы. [2] |
Константы Михаэлиса для реакций L - - DL и D-DL могут быть вычислены из результатов, представленных на рис. 6 - 4, и равны / а 9 7 - 10 - 4 моль / л и / Со 4 6 - 10 - 4 моль / л соответственно, а максимальные скорости VL 2 22 моль / ч и VD 0 95 моль / ч соответственно. [3]
Константа Михаэлиса для 3-фосфоглицеринового альдегида Км 3 9 10 4Л /; активность очень высока: 1 моль фермента при 26 катализирует превращение 945 000 молей субстрата в минуту. Активность фермента подавляется ионами фосфата. Фермент широко распространен в животных тканях и играет важную роль в процессе гликолиза, обеспечивая утилизацию фосфодиоксиацетона. [4]
Константа Михаэлиса имеет большое значение при изучении ферментативных реакций, так как она служит мерой сродства между ферментом и субстратом: чем больше их способность к образованию комплекса ES, тем меньше Km, и наоборот. Значение константы Михаэлиса зависит от природы исследуемого фермента, а в тех случаях, когда он действует на несколько субстратов, - и от природы субстрата, на который он действует. [5]
Константа Михаэлиса в определенной мере характеризует сродство фермента к субстрату. Так как эта величина является аналогом константы диссоциации комплекса ES, то чем ниже Кц, тем выше сродство. [6]
 |
Определение Км и Vmsx методом двойных обратных величин.| Определение Км и Vm, методом Эди-Хофсти. [7] |
Константа Михаэлиса имеет большое значение при исследовании ферментов; она является весьма важным параметром, характеризующим, в частности, степень сродства фермента к субстрату. [8]
Константа Михаэлиса ( Км) - Концентрация субстрата, при которой скорость ферментативной реакции равна половине ее максимальной скорости. [9]
Константа Михаэлиса для 3-фосфоглицеринового альдегида Км 3 9 10 - 4Af; активность очень высока: 1 моль фермента при 26 катализирует превращение 945 000 молей субстрата в минуту. Активность фермента подавляется ионами фосфата. Фермент широко распространен в животных тканях и играет важную роль в процессе гликолиза, обеспечивая утилизацию фосфодиоксиацетона. [10]
Константы Михаэлиса ( Кт) для фиксации N2 неповрежденными клетками Azotobacter vine-landii, сине-зеленой водорослью Nostoc mus - согит и изолированными корневыми клубеньками соевых бобов составляют от 0 020 до до 0 025 атм. [11]
Константа Михаэлиса Км ( &2 ka) / ki представляет собой константу диссоциации комплекса Мо - ГПЭБ. Найденная графически из зависимости 1 / W - 1 / [ ГПЭБ ] при начальных концентрациях гидроперекиси она оказалась равной 90 96 моль / л, тогда как константа скорости определяющей стадии ka 1 39 л / моль - сек. Графическое определение констант диссоциации комплексов Мо-вода иМо - метилфенилкарбинол показало, что ингибирование реакции водой в 25 - 26 раз сильнее, чем метилфенилкарбинолом. Наиболее активным ингибитором признана вода, эффект ингибирования которой в 12 - 25 раз больше, чем у спиртов, образующихся при распаде гидроперекисей. При исследовании относительной ингибирующей активности спиртов различного строения найдена корреляция полярных факторов по Тафту ( а) с константами диссоциации комплексов этих спиртов с катализатором. [12]
Константу Михаэлиса определяют следующим способом. Экспериментальные данные представляют в виде кривой, подобной той. По этому графику находят на оси абсцисс концентрацию субстрата, при которой скорость реакции равна половине максимальной. Гораздо удобнее представлять опытные данные таким способом, чтобы график зависимости был дан в виде прямой. [13]
Обе константы Михаэлиса имеют, как мы видели, ясный и простой физический смысл. [14]
Зависимость констант Михаэлиса / с3 и Км от рН может быть весьма сложной. Поэтому для исследования зависимости от рН среды требуется использование буферных растворов. При этом нередко оказывается, что между компонентами буферного раствора ( особенно НРО) и ферментом имеется определенное взаимодействие. Кроме того, влияние на активность белка и активность субстрата также оказывает ионная сила раствора, что еще в большей степени усложняет интерпретацию процесса в буферном растворе. [15]
Страницы: 1 2 3 4