Константа - михаэлис
Cтраница 3
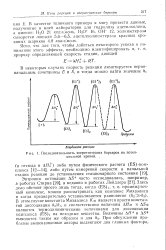 |
Последовательность энергетических барьеров на потенциальной кривой. [31] |
В этом случае константа Михаэлиса Км является просто константой диссоциации k2 / kl, и соответственно величины АНм и Д5уи являются термодинамическими величинами для диссоциации комплекса ( ES) i на исходные вещества. [32]
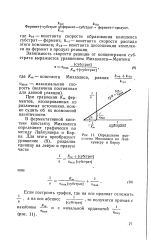 |
Определение константы Михаэлиса по Лай-нуиверу и Бэрку. [33] |
В ферментативной кинетике константу Михаэлиса определяют графически по методу Лайнуивера и Бэр-ка. [34]
Кш представляет собой константу Михаэлиса, являющуюся экспериментально определяемой величиной. [35]
Cm ( называется константой Михаэлиса) - константа диссоциации в реакции образования комплекса фермент - субстрат. Как и все константы диссоциации, константа Михаэлиса имеет размерность концентрации и при v / 2VxaKC величина S Km - Таким образом, Km равна концентрации субстрата, при которой скорость реакции составляет половину максимальной. [36]
Это значит, что константа Михаэлиса численно равна концентрации субстрата, при которой стационарная скорость ферментативной реакции равна половине максимальной скорости. [37]
Член / См, константа Михаэлиса - Ментен, в данном конкретном примере выражает константу диссоциации. В настоящей книге / См рассматривается как концентрация субстрата, при которой скорость реакции равна половине максимальной. [38]
 |
Возможные пути восстановления изонитрилов в углеводороды в присутствии молибденовых комплексов. [39] |
Если учесть, что константа Михаэлиса / См для изонитрилов обычно в 10 - 100 раз больше в случае модельных комплексов, чем для фермента, следует сделать вывод, что модели характеризуются гораздо меньшим сродством к субстрату, чем сами ферменты. Как отметили авторы работы [137], это, по-видимому, отражает различия в я-акцепторных и о-донорных свойствах атомов металла в модели и в ферменте. Можно ожидать, что связывание таких ли-гандов, как N2, CO, изонитрилы и ацетилены, существенно зависит от слабых изменений донорно-акцепторных свойств связывающего центра. Последние можно варьировать путем введения вспомогательных лигандов. Исходя из этих соображений, Хилл и Ричарде [143] показали, что система, основным компонентом которой является МоО42 и которая включает в свой состав Fe ( II) и 2-аминоэтантиол, дает выход аммиака 15NH3 из 15N2, в 30 раз превышающий выход аммиака в присутствии цистеина в качестве лиганда молибдена. Описанные выше модельные исследования показывают, что сочетание молибдена с тиоловыми лигандами дает весьма эффективную гомогенно-каталитическую систему, обладающую необходимой способностью связывать и восстанавливать субстраты. [40]
Полученная константа и есть константа Михаэлиса. [41]
Объединенная константа Кт называется константой Михаэлиса. [42]
Константу / См называют константой Михаэлиса - Ментена. Она характеризует зависимость скорости ферментативной реакции от концентрации субстрата в стационарном состоянии про-цесса. [43]
Для сульфатов меди и никеля константы Михаэлиса составляют 0 12 и 0 045 соответственно. [44]
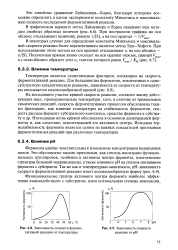 |
Зависимость скорости ферментативной реакции от температуры.| Зависимость скорости реакции от рН. [45] |
Страницы: 1 2 3 4