Константа - михаэлис
Cтраница 4
В некоторых случаях для определения константы Михаэлиса и максимальной скорости реакции более перспективным является метод Эди-Хофсти. [46]
Величина - k 3 называется константой Михаэлиса и обозначается через Km. [47]
Здесь Km есть уже известная нам константа Михаэлиса. Если действие ингибитора имеет обратимый, но неконкурентный характер, ингибитор способен реагировать как с ферментом, так и с ферментно-субстратным комплексом. [48]
Вследствие флуктуации зарядов должны изменяться и константа Михаэлиса ( см. стр. [49]
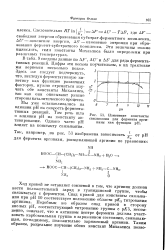 |
Изменение копстанты связывания для фермента аргиназы как функции рН. [50] |
Эти величины можно выялслнть, если константы Михаэлиса были определены при различных температурах. [51]
На рис. 93 приведена плотность распределения констант Михаэлиса в ферментативном катализе. Для фермент-субстратного взаимодействия в большинстве случаев характерно связывание с константой диссоциации, большей чем КИМ. [52]
Следовательно, в этом случае изменение константы Михаэлиса для разных субстратов будет обусловлено лишь изменением одной этой константы скорости. Точка, которая на рисунке остается ниже прямой, соответствует пространственно затрудненному о-нитрофениловому эфиру. [53]
Наличие такой стадии не проявляется в константе Михаэлиса, но приводит к уменьшению наблюдаемой каталитической константы скорости. [54]
Величина У ( м, называемая константой Михаэлиса, представляет собой константу стационарного состояния, величину, характеризующую сродство комплекса к субстрату в процессе течения реакции. Эта характерная для данного фермента величина ( постоянная при определенных условиях), может быть определена экспериментально и является наиболее важной константой в химии ферментов. [55]
V 2 8 в ( Км - константа Михаэлиса) и зависит от начальной концентрации фермента СЕ в первой степени, а зависимость от концентрации субстрата С5 не степенная. [56]
Сумма всех этих способов связывания задает величину константы Михаэлиса, а график зависимости 1 / Дт п от п - / 1 ( при вариации степени полимеризации субстрата п) позволяет определить величину константы ассоциации субстрата с ферментом при заполнении всех сайтов как тангенс угла этой зависимости ( см. уравнение 46), если протяженность активного центра известна. [57]
Высокое сродство дегидрогеназ к стероидам иллюстрируется значениями констант Михаэлиса: для 1 2-дегидрогеназ из Nocardia restrictus [110] и Pseudomonas testosteroni [34] Ки-2 5 10 - Б М ( андростен - дион), а для 4 5а - дегидрогеназы из P. Максимальная активность ферментов во всех трех случаях связана с концентрацией субстрата порядка 1 10 - М при более высоких концентрациях стероиды проявляют ингибирующее действие. [58]
Из данных таблицы следует, что значения констант Михаэлиса для субстратов весьма существенно различаются по скорости ферментативного гидролиза и колеблются не в столь больших пределах, как V. Кроме того, скорость ферментативного процесса не находится в простой связи с константой Михаэлиса: с увеличением К т она не падает, а возрастает. [59]
Страницы: 1 2 3 4