Константа - михаэлис
Cтраница 2
Значение константы Михаэлиса может быть использовано для определения концентрации субстрата, необходимой для получения максимальной скорости реакции, а так же при решении вопроса об идентичности ферментов, полученных из различных источников. Для различных классов ферментов значения константы Михаэлиса обычно сильно отличаются. В табл. 29 приведены значения константы Михаэлиса для некоторых ферментов. [16]
Зависимость констант Михаэлиса / с3 и Км от рН может быть весьма сложной. Поэтому для исследования зависимости от рН србды требуется использование буферных растворов. При этом нередко оказывается, что между компонентами буферного раствора ( особенно НРО) и ферментом имеется определенное взаимодействие. Кроме того, влияние на активность белка и активность субстрата также оказывает ионная сила раствора, что еще в большей степени усложняет интерпретацию процесса в буферном растворе. [17]
 |
График зависимости [ S ] / P от концентрации субстрата в случае гидролиза карбобензоксиглициллейцина ( определение константы Михаэлиса по Л айнуиверу - Бэрку. [18] |
Величины константы Михаэлиса для различных ферментных реакций бывают очень разными. Большая константа показывает, что связь между субстратом и ферментом непрочна. [19]
Рассчитать константу Михаэлиса, пользуясь графическим методом Лайнуивера и Бэрка. [20]
Следовательно, константа Михаэлиса численно равна такой концентрации субстрата, при которой скорость ферментативной реакции равна половине максимальной. [21]
Кт - константа Михаэлиса - служит важной характеристикой фермента. [22]
Существует так называемая константа Михаэлиса / См, характерная для каждого отдельного фермента; ее можно определить экспериментально и вывести математически. Числовое выражение Km равно концентрации субстрата, при которой скорость действия фермента составляет половину от той максимальной скорости vmax, которую можно получить, если насытить фермент его субстратом. Отсюда ясно, что при концентрации субстрата, которая соответствует / См, фермент может проявить лишь половину своего наибольшего эффекта. [23]
Определите значения константы Михаэлиса и максимальной скорости для гидролиза метилового эфира N-ацетил - Ь - валина, катализируемого а-химотрипсином. [24]
Кажущаяся величина константы Михаэлиса для субстратов ( фрук-тозо-6 - фосфата и АТФ) зависит от рН реакционной среды, в которой проводится определение ферментативной активности и от концентрации второго субстрата. [25]
Предполагаемая величина константы Михаэлиса ферментативной реакции, в которой участвует УДФ-О-галактуроновая кислота, равна 1 7 - 10 - 6 М, и при концентрации субстрата 3 7 - 10 5 моль / л скорость катализируемой ферментом полимеризации D-галактуроновой кислоты составляет 4 7 - 10 - 9 моля на 1 мг белка в минуту. Фермент может самопроизвольно инактивироваться. [26]
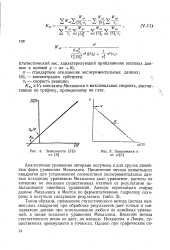 |
Зависимости [ S ] / o от [ S ].| Зависимости v от t / [ S ]. [27] |
Ст и Fo константа Михаэлиса и максимальная скорость, рассчитанные по графику, проведенному на глаз. [28]
При первоначальных исследованиях константа Михаэлиса, о чем уже говорилось выше, воспринималась как константа диссоциации комплекса фермент - субстрат и, естественно, по аналогии с константами диссоциаций в других обратимых реакциях была предложена для оценки сродства субстрата к ферменту. [29]
В этом случае константа Михаэлиса уже не является константой равновесия, а представляет собой комбинацию кинетических констант. [30]
Страницы: 1 2 3 4