Константа - скорость - распад
Cтраница 3
Величина k называется константой скорости распада и характеризует скорость радиоактивного превращения. [31]
Было найдено, что константа скорости распада ka не зависит от давления при временах между столкновениями, изменяющихся от 2 - 10 - 13 до 10 - 8 с. [32]
При 105 5 С константа скорости распада ди-трет. [33]
При температуре 130 С константа скорости распада ди-трет. [34]
В работе [163] измерена константа скорости распада аммиака в широ. Результаты измерений удовлетвори 1ельно объясняются в рамках теории Ра т са - Рамспергера - Касселя - Маркуса. [35]
Другой характер носит зависимость константы скорости распада дигидропероксида от соотношения компонентов катализатора. [36]
Из таблицы видно, что константы скорости распада этих инициаторов превышают константу скорости распада перекиси бензоила на два порядка и более. [37]
Следует отметить невероятно большие предэкспоненты констант скоростей распада. Однако, несмотря на их неудовлетворительную количественную сторону, они качественно ярко свидетельствуют о роли системы сопряжения. [38]
Стабильность радикалов ( и соответственно значение константы скорости распада перекиси) возрастает при введении электронодонорных групп и уменьшается при введении электроно акцепторных групп. [39]
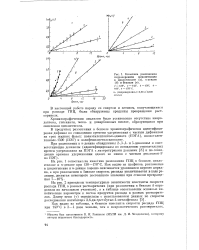 |
Кинетика разложения гидроперекиси циклогексила в циклогексане ( а, и-декано ( б и бензоле ( в. 1 - 130, 2 - 140, з - 150, 4. [40] |
На рис. 2 приведены температурные зависимости константы скорости распада ГПЦ в разных растворителях ( при разложении в бензоле k определяли по начальным участкам), а в таблице сопоставлены основные кинетические параметры и состав продуктов распада в разных растворителях. [41]
В первом приближении предэкс-поненты в значениях констант скорости распада углеводородной молекулы по различным связям одинаковы, следовательно, с наибольшей скоростью молекула распадается на радикалы по наименее прочной связи. [42]
Близость Bi к единице означает, что константы скорости распада парафинов и олефинов имеют один порядок. Это подтверждает наше соображение о том, что учет вторичных реакций распада олефинов обязателен. [43]
Как видно из таблицы, в бензоле константа скорости распада ГПЦ при 140 С в 3 - 4 раза меньше, чем в неароматических растворителях. [44]
Gl) показывает, что для нахождения константы скорости распада иногда ( при х & 10) можно обойтись без непосредственного нахождения функции распределения р ( х, t), которое является обычно достаточно сложной задачей, и можно решать более простую задачу о среднем времени достижения границы. [45]
Страницы: 1 2 3 4