Бимолекулярная константа - скорость
Cтраница 2
Таким образом, любое изменение бимолекулярной константы скорости в зависимости от магнитного поля приводит к соответствующей модуляции замедленной флуоресценции. Можно показать, что при промежуточных значениях магнитного поля, т.е. когда 0 Н 1 кГс, шесть из девяти возможных промежуточных парных состояний имеют синглетную компоненту. Аналогично объясняется уменьшение интенсивности замедленной флуоресценции и положение резонансов в сильном магнитном попе. [16]
Выше было приведено уравнение для вычисления бимолекулярной константы скорости необратимой реакции фермента с ингибитором. В соответствии с этим уравнением бимолекулярная константа скорости реакции может быть вычислена, если известны начальные молярные концентрации фермента и ингибитора и убыль концентрации одного из реагирующих компонентов ( обозначим ее xt) во времени. [17]
В системе с одинаковыми начальными концентрациями реагентов а бимолекулярная константа скорости выражается через время полупревращения U / 2 уравнением (6.39), к2 1 / ( / 2а), так что кинетику очень быстрых реакций можно изучить, работая с очень малыми концентрациями. [18]
В системе с одинаковыми начальными концентрациями реагентов а бимолекулярная константа скорости выражается через время полупревращения г / 2 уравнением (6.39), &2 1 / ( Ь / а), так что кинетику очень быстрых реакций можно изучить, работая с очень малыми концентрациями. [19]
АВ - разрыхленный комплекс, тогда как k3 - бимолекулярная константа скорости, которая может иметь некоторую энергию активации. [20]
Поэтому, согласно теории Бренстеда - Бьеррума, логарифм бимолекулярной константы скорости для данной реакции является линейной функцией от квадратного корня из ионной силы раствора, а наклоны графиков, построенных в этих координатах, для различных ионных реакций в одном и том же растворителе и при одной и той же температуре относятся между собой как небольшие целые числа. [21]
Поэтому, согласно теории Бренстеда - Бьеррума, логарифм бимолекулярной константы скорости для данной реакции является линейной функцией от квадратного корня из ионной силы раствора, а наклоны графиков, построенных в этих координатах, для различных ионных реакций в одном и том же растворителе и при одной и той же температуре относятся между собой как небольшие целые числа. [22]
АВ - разрыхленный комплекс, тогда как k3 - - - бимолекулярная константа скорости, которая может иметь некоторую энергию активации. [23]
Наиболее исчерпывающая теория модуляции внешним магнитным полем Т - / - бимолекулярной константы скорости была развита в работе Су-ны [359], в которой пространственная зависимость волновых функций трип-летного экситона учитывается в явном виде. В этой теории пространственными переменными волновой функции триплетных экситонов пренебрегают и процесс аннигиляции экситонов рассматривается кинетически. [25]
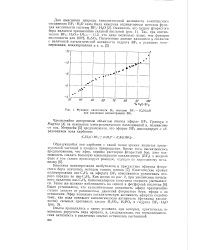 |
Функция кислотности Но системы BF3 - ( С2Н5 2О при различных концентрациях ВРз. [26] |
Как видно из рис. 2, при увеличении начального давления изо - С4Н8 бимолекулярная константа скорости уменьшается. Было установлено, что каталитическая активность эфира чрезвычайно сильно зависит от равновесных давлений фтористого бора, эфира и их отношения. [27]
 |
Два типа реакций замещения. [28] |
Было показано, что в течение одного кинетического опыта реакция идет как бимолекулярная [6], однако значение бимолекулярной константы скорости возрастало с ростом начальной концентрации соли. Было высказано мнение [20], что кинетику этого процесса невозможно объяснить без участия анионов в лимитирующей стадии. [29]
 |
Два типа реакций замещения. [30] |
Страницы: 1 2 3 4