Бимолекулярная константа - скорость
Cтраница 4
Было показано, что эта реакция относится к медленным. В двух типичных инертных растворителях бимолекулярные константы скорости равны: к2 9 16 X 10 ехр [ - 12 400 / ( RT) ] в гексане и к % 4 14 X 105 ехр [ - 13 A00 / ( RT) ] в четыреххлористом углероде. [46]
Отсюда был сделан принципиальной важности вывод о том, что в основе механизма ингибирования холинэстераз фос-форорганическими соединениями лежит необратимая химическая реакция бимолекулярного механизма. При этом оказалось, что бимолекулярные константы скорости ингибирования холинэстераз имеют, как правило, очень большие величины. [47]
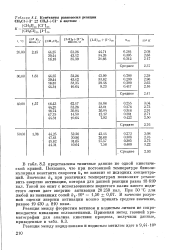 |
Константы равновесия реакции CHgCI - j - I - j CH3I CI - в ацетоне. [48] |
В табл. 8.2 представлены типичные данные по одной кинетической кривой. Показано, что при постоянной температуре бимолекулярная константа скорости / с2 не зависит от исходных концентраций. Значения к2 при различных температурах позволяют установить энергию активации, которая для данной реакции равна 18 610 кал. Такой же опыт с использованием йодистого калия вместо йодистого лития дает энергию активации 20 250 кал. В качестве разумной оценки энергии активации можно принять среднее значение, равное 19 430 810 ккал. [49]
 |
Константы равновесия реакции CHgCl - j - I - СН31 СГ - в ацетоне. [50] |
В табл. 8.2 представлены типичные данные по одной кинетической кривой. Показано, что при постоянной температуре бимолекулярная константа скорости k2 не зависит от исходных концентраций. Значения kz при различных температурах позволяют установить энергию активации, которая для данной реакции равна 18 610 кал. Такой же опыт с использованием йодистого калия вместо йодистого лития дает энергию активации 20 250 кал. В качестве разумной оценки энергии активации можно принять среднее значение f равное 19 430 810 ккал. [51]
Наоборот, при изучении крекинга бутадиена статическим методом необходимо применять бимолекулярную константу скорости крекинга Вогена, учитывающую начальную концентрацию бутадиена. [52]
Процессы испускания света и внутримолекулярные безызлучательные процессы являются процессами первого порядка с константами скорости, обратными времени жизни. Эти процессы имеют второй порядок, однако поскольку концентрация тушащего вещества во много раз выше концентрации возбужденных молекул, их характеризуют константой скорости первого порядка kq [ Q ], где kg - бимолекулярная константа скорости, a [ Q ] - концентрация тушащих молекул. С внутренней конверсией из верхних состояний конкурируют лишь очень быстрые химические превращения этих состояний. [53]
За исключением поглощения света, все рассмотренные выше процессы являются реакциями первого порядка с константами скорости, обратными приведенным на рис. 23 временам жизни. Эти процессы, естественно, будут иметь второй порядок, однако, поскольку концентрация тушащего вещества часто гораздо выше концентрации возбужденных молекул, их можно характеризовать константами скорости первого порядка kQ [ Q ] или kq [ q ], где kQ и kq - бимолекулярные константы скорости, a [ Q ] и [ q ] - концентрации тушащих молекул. [54]
Последнее соображение, которое часто приводят для различных жидких систем, основано на вычислении константы скорости лимитируемого диффузией процесса по уравнению Дебая [231] ( см. разд. Вычисленные значения константы диффузии для бензола и хлороформа при 20 равны 1 0 - 1010 и 1 1 - 1010 л / моль-сек соответственно. Величину примерно К) 10 полезно запомнить как бимолекулярную константу скорости лимитируемого диффузией процесса в подвижных жидкостях при комнатной температуре. [55]
 |
Кинетические параметры и влияние электролитов на реакцию между тиосульфатом и бромацетатом в воде при 25. С. [56] |
Значение [ М2 ] поддерживается постоянным в течение всего хода реакции, так что реакция все время остается бимолекулярной. Константы диссоциации Кг и Кг получают независимым путем из точных кондуктометрических измерений в отсутствие химических реакций, как описано в гл. Из этих данных уже можно определить отдельно все три бимолекулярные константы скорости. На рис. 7.2 показаны графики зависимости lg k - 2 и lg ka от ионной силы. [57]
 |
Кинетические параметры и влияние электролитов на реакцию между тиосульфатом и бромацетатом в воде при 25. С. [58] |
Значение [ М2 ] поддерживается постоянным в течение всего хода реакции, так что реакция все время остается бимолекулярной. Константы диссоциации Кг и К 2 получают независимым путем из точных кондуктометрических измерений в отсутствие химических реакций, как описано в гл. Из этих данных уже можно определить отдельно все три бимолекулярные константы скорости. На рис. 7.2 показаны графики зависимости lg kt и lg ka от ионной силы. [59]
Страницы: 1 2 3 4