Каталитическая константа
Cтраница 1
Каталитические константы коррелируют с константами ассоциации сульфитного дианиона с кислотами и катионами. Это может означать, что катализ осуществляется за счет стабилизации дианионного переходного состояния путем образования водородных связей. [1]
Каталитические константы, равные величине k при [ Н3О ] 1 или ОН - 1, характеризуют каталитическое влияние диссоциирующих кислот и оснований, независимо от их природы, на скорость той или иной реакции. [2]
Каталитические константы для кислот в водном растворе хорошо коррелируют с р / С, причем заметного различия между незаряженными и катионными кислотами ( карбоновые кислоты и катионы пиридиния) не наблюдается. Для 2 6-замещенных ионов пиридиния наблюдается некоторое замедление реакции вследствие стерических факторов. Каталитические константы для оснований несколько менее точны, и, как показали Грюн и МакТигью [49], ошибка обусловлена методом измерения скоростей реакций по образованию продуктов присоединения между ацетальдегидом и анионом катализатора. Можно отметить, что более ранние измерения при 0 дилатометрическим методом [ 10J дали лучшую корреляцию между kb и р / С семи оснований различных типов, поэтому необходимы дальнейшие исследования. [3]
Каталитические константы, измеренные в 95 % - ном водном диоксане, сравнивали с величинами р / С катализаторов в воде. В число 24 кислот ( табл. 3) входят главным образом карбоновые кислоты и, кроме того, азотная кислота, о-хлорфенол и вода. [4]
Значение каталитической константы, найденное в стационарном режиме проведения реакции ферментативного гидролиза, равно 0 03 сек-1. [5]
Зависимость каталитической константы скорости гидролиза этилового эфира М - ацетил - Ь - тирозина, катализируемого а-химотрипсином. [6]
Малая чувствительность каталитической константы скорости к силе кислот, по-видимому, объясняется образованием комплекса кислота - катализатор, нуклеофильность которого намного выше, чем у свободной кислоты, что согласуется с полученными нами ранее [2] данными о кинетике реакции окиси пропилена с метакриловой кислотой при катализе РеС13: нулевой порядок по кислоте, первый - по окиси и катализатору. [7]
Бренстед я Педерсен измерили каталитические константы пятнадцати карбоксилат-ионов и двух фосфат-ионов. [8]
Если по гипотезе Хироми каталитическая константа пропорциональна гидролитическому коэффициенту k0, который является строго характеристическим для данного фермента, и определяется исключительно соотношением констант ассоциации субстрата в продуктивном и непродуктивном фермент-субстратном комплексах ( 17), то по гипотезе Тома величина гидролитического коэффициента зависит от способа связывания фермента с субстратом и от степени полимеризации последнего. На наш взгляд, это придает настолько большую гибкость расчетам па основании концепции Тома, в особенности с помощью машинного анализа, что может в отдельных случаях делать бессмысленными определения показателей сродства индивидуальных сайтов активного центра - фермента, поскольку все наблюдаемые кинетические эффекты могут быть объяснены в рамках вариации гидролитического коэффициента при изменении структуры олигомерного субстрата и способов его связывания с ферментом. [9]
Интересно проанализировать численные значения каталитических констант скоростей и констант Михаэлиса различных ферментов с тем, чтобы представить средние скорости реакций в биохиминеских системах. [10]
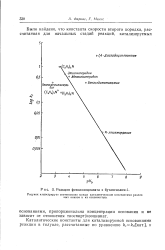 |
Реакция фенилизоцианата с бутантиолом-1. [11] |
Рисунок иллюстрирует соотношение между каталитическими константами различных аминов и их основностью. [12]
Кн и / Сон - каталитические константы соответственно водородного и гидроксильного ионов. [13]
В этих условиях равновесие ухудшает каталитическую константу и улучшает эффективную константу Михаэлиса. [14]
Число активных центров Число оборотов равно каталитической константе, если молекула фермента состоит только из одной полипептидной цепи и если каждая ферментная молекула реагирует в данный момент времени только с одной молекулой субстрата. В действительности, однако, молекулы многих ферментов состоят из нескольких субъединиц и содержат более одного каталитически независимого активного центра. [15]
Страницы: 1 2 3 4