Кажущаяся константа - равновесие
Cтраница 3
Подстановка уравнения ( 26) в уравнения типа ( б), ( 12) или ( 13) позволяет получить теоретическую зависимость величины кажущейся константы скорости ( & каж) или кажущейся константы равновесия ( Ка каж) от концентрации ПАВ для реакции с участием ионного реагента. [31]
Подставляя произвольные концентрации реагентов и продуктов в выражение для константы равновесия, как было сделано выше, мы получим кажущуюся константу равновесия, которую обозначают буквой Q. Кажущаяся константа равновесия становится равной истинной константе равновесия К только тогда, когда концентрации всех компонентов реакционной системы достигнут своих равновесных значений, короче говоря, Q К только при равновесии. Мы убедились, что если кажущаяся константа равновесия больше К, то вещества, указанные в правой части химического уравнения реакции, должны реагировать с образованием веществ, указанных в его левой части, другими словами, реакция приближается к равновесному состоянию, смещаясь справа налево. Короче, если Q К, реакция сдвигается справа налево. [32]
Изучение поликонденсации гексаметиленаммонийадипината в присутствии воды при 200 - 220 С показало, что данный процесс протекает очень быстро и равновесие в нем достигается в течение 5 час. Кажущаяся константа равновесия и среднечисловой молекулярный вес полиамида увеличиваются с ростом температуры и с уменьшением содержания в системе воды. Поликонденсация гексаме-тилендиаммонийадипината в присутствии воды протекает как реакция второго порядка, с энергией активации 22 ккал / моль. В присутствии больших количеств воды данная поликонденсация является эндотермической реакцией. [33]
Константа равновесия позволяет предсказывать, является ли самопроизвольной данная реакция при конкретных условиях, а также вычислять концентрации реагентов и продуктов при равновесии. Кажущаяся константа равновесия Q определяется точно таким же выражением, что и действительная константа равновесия - Крав, но Q применима и к неравновесным условиям. Если при заданных условиях Q меньше Кравн, самопроизвольно должна протекать прямая реакция. Если же Q больше Кравн, самопроизвольной должна быть обратная реакция. Когда Q Крав, система находится в равновесии. [34]
Выражение ( 16 - 21) имеет более общий вид, чем использовавшееся ранее выражение ( 4 - 10) для кажущейся константы равновесия, и позволяет получить более полное представление о равновесии. Кажущаяся константа равновесия Q может быть вычислена для любых экспериментальных условий по данным о парциальных давлениях реагентов и продуктов. [35]
Если кажущаяся константа равновесия меньше истинной константы равновесия, реакция протекает самопроизвольно в сторону образования продуктов. Когда кажущаяся константа равновесия совпадает с Кр вн) прямая и обратная реакции протекают с одинаковой скоростью и химическая система находится в положении равновесия. [36]
В расчет поэтому вводится кажущаяся константа равновесия данной реакции. Отношение кажущейся константы равновесия к истинной устанавливается на основе экспериментальных данных. [37]
Сложнее обстоит дело с исследованием сильно диссоциирующих комплексов, когда константы равновесия реакций комплексообразования соизмеримы с поправочными множителями. В таких случаях кажущиеся константы равновесия существенно отличаются от истинных. Отсюда следует, что к результатам изучения слабых комплексов с помощью графических приемов, основанных на использовании уравнения (11.12) для кажущейся константы равновесия ( см. разд. Поскольку при этом оба параметра, лгк и Кс, определяются одновременно, неправильное исходное выражение для константы равновесия может заметно исказить величину физического параметра комплекса. [38]
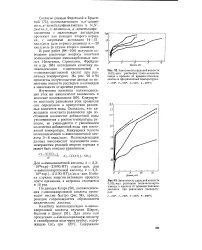 |
Зависимость удельной вязкости 0 5 % - ных растворов поли-ш-энанто-амида в крезоле от времени поликонденсации при различных температурах. [39] |
Оказалось, что кажущаяся константа равновесия при постоянном количестве добавленной воды увеличивается с ростом температуры реакции, но уменьшается с увеличением количества добавленной воды при постоянной температуре. Кажущаяся теплота поликонденсации оаминоэнантовой кислоты 3 - 6 ккал / моль. [40]
Изменение свободной энергии газовой реакции зависит от парциальных давлений ее компонентов по уравнению AG AG RTlnQ. Величина Q представляет собой кажущуюся константу равновесия, определение которой было введено в гл. [41]
Элементы без переноса используют в осн. Элементы с переносом используют для определения кажущихся констант равновесия ( поскольку при этом не учитывают жидкостной потенциал), активностей и коэф. [42]
Это важное соотношение связывает константу равновесия реакции со стандартным изменением свободной энергии для данной реакции. Константа равновесия, К т, совпадает с кажущейся константой равновесия, относящейся к условиям равновесия. [43]
Рассмотрим подробнее выражение в скобках. Оно представляет собой отношение активностей продуктов к активностям реагентов и совпадает с кажущейся константой равновесия Q, введенной в гл. [44]
Это безразмерная величина, не зависящая от концентрации. На практике вместо активностей часто измеряют концентрации, так что отношение концентраций, или кажущаяся константа равновесия, зависит от концентрации. Но если такие кажущиеся константы равновесия К экстраполировать к бесконечному разбавлению ( когда все у равны 1), можно найти истинную константу равновесия. Таким образом, измеряя константы равновесия при различных температурах, можно найти ДЯ для реакции. [45]
Страницы: 1 2 3 4