Истинная константа - скорость
Cтраница 1
 |
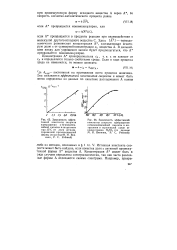
Зависимость эффективной константы скорости превращения о-бензоилбен. шмной кислоты в антрахинон при 35 С от доли дегидратированной прото-нированной формы ( по данным М. И. Винника, Р. И. Рябовой. [1] |
Истинная константа скорости может быть найдена, если известна доля а активной промежуточной формы S вещества S. Концентрация S может быть в ряде случаев определена спектроскопически, так как часто различные формы S отличаются своими спектрами. [2]
 |
Зависимость эффективной константы скорости превращения о-бензоилбепзойной кислоты в антрахинон при 35 С от доли дегидратированной прото-нированной формы ( по данным М. И. Винника, Р. И. Рябовой. [3] |
Истинная константа скорости л о: кст ыть найдена, егли известна доля а активной промежуточной формы S вещьства S. Концентрация S может быть в ряде случаев определена спектроскопически, так как часто различные формы S отличаются своими спектрами. [4]
Истинная константа скорости может быть найдена, если известна доля а активной промежуточной формы А вещества А. Концентрация А может быть в ряде случаев определена спектроскопически, так как часто различные формы А отличаются своими спектрами. [6]
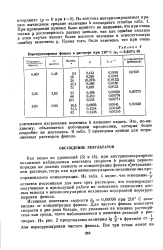 |
Перегруппировка фенола в растворе при 210 С ( х 3 623 % D. [7] |
Истинная константа скорости k0 0 00090 при 210 С независима от концентрации фенола. На рис. 2 представлены величины lg - - в функции от - - для перегруппировки чистого фенола. [8]
B Истинная константа скорости из кинетических измерений найдена быть не может. Для ее определения нужно независимым путем определить константу основности А. [10]
Ср - истинная константа скорости реакции, отнесенная к единице его объема; Y - модуль Тиле ( см. гл. [11]
Это не обязательно истинная константа скорости элементарного процесса, и в частном случае, когда продукт А расходуется в реакциях окисления, ka может быть функцией давления кислорода над полимером. [12]
Что касается истинной константы скорости в клетке, то нет оснований считать, что общая структура выражения для нее принципиально отличается от полученной для реакции в газовой фазе. Действительно, для протекания реакции нужны и встреча находящихся в клетке частиц, учитываемая фактором соударений, и наличие у соударяющихся частиц достаточной энергии для преодоления энергетического барьера, учитываемое экспоненциальным множителем ехр [ - E / ( RT) ], и определенная ориентация реагирующих частиц, учитываемая стерическим фактором. Наиболее существенное изменение претерпевает понятие фактора соударений, так как встреча частиц определяется скорее всего колебаниями частиц в пределах клетки. [13]
Для нахождения истинных констант скорости, не искаженных влиянием двойного слоя, необходимо определяемые непосредственно из опыта кажущиеся значения частных констант протонизации k ( равные наклону прямых зависимости р от концентрации данного донора протонов раствора) экстраполировать к бесконечно большой толщине реакционного слоя, при которой не сказывается влияние поля электрода. Эта зависимость для объемных каталитических волн имеет прямолинейный характер [87], и величина k, экстраполированная к [ H ] - 1 - 0, отвечает истинной константе скорости пере-дачи протона от донора к молекуле катализатора. [14]
Определены наблюдаемые и истинные константы скорости процесса. Найдена энергия активации Е, составляющая 40 ккал / моль для материала ГМЗ. [15]
Страницы: 1 2 3 4