Доказательство - механизм
Cтраница 2
Факт осуществления асимметрического синтеза можно рассматривать как доказательство механизма дебромирования, при котором образуются хиральные карбеноидные промежуточные соединения ( см. также разд. [16]
Постоянство данной величины в процессе образования каждого силиката является доказательством механизма превращения кремнезема в силикат, предусматривающего переход сорбента в раствор. [17]
Несмотря на то что частичная фрагментация указывает па постадийный процесс, доказательство механизма можно получить только путем комбинированного исследования продуктов и скоростей на основе следующего критерия: в постадийном процессе - заместитель должен заметно влиять на состав продуктов, но только слабо - на скорость, с которой продукты образуются. [18]
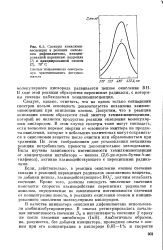 |
Спектры хемилюми-несценции в реакции окисления дифенилметана, инициированной перекисью лауроила ( 1 и инициированной озоном ( 2, 70 С. [19] |
Следует, однако, отметить, что на одном только совпадении спектров нельзя основывать доказательство механизма хемилю-минесценции при окислении озоном. Допустим, что в реакции окисления озоном образуется свой эмиттер хемилюминесценции, который не является продуктом реакции окисления молекулярным кислородом. В этом случае спектры тоже могут совпадать, если возможен перенос энергии от озонного эмиттера на продукты окисления, которые в небольших количествах могут сохраняться в окисляемом веществе после очистки или образовываться при хранении. [20]
Автор считает, что восстановительное действие реактива Гриньяра на метоксисилан R3Si OCHs - одно из наиболее убедительных доказательств четырехцентрового механизма для реакций ( в неполярных средах), затрагивающих связи Si - О. [21]
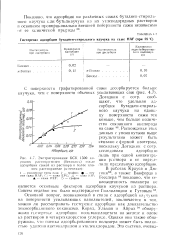 |
Экстрагирование БСК 1500 хорошим растворителем ( бензолом после адсорбции сажей из раствора в более плохом растворителе ( н-гептане. [22] |
Основной вопрос, возникающий в связи с адсорбцией ка чуков на поверхности усиливающих наполнителей, заключается в том, можно ли рассматривать гистерезис адсорбции как доказательство хемосорбцпонного механизма. [23]
Следует, однако, учитывать, что образование циклической структуры может происходить в результате вторичных реакций с участием А1 - органического компонента [ ш ], и поэтому ее наличие нельзя рассматривать как доказательство механизма роста цепи. [24]
Механизм SN2 ( P), названный по аналогии с 5к2 - замещени-ем у насыщенного атома углерода, включает одновременный раз-рыв связи и образование новой связи в переходном состоянии, имеющем две длинные pd - связп и три более короткие 5р2 - связи ( схема 4 а); Доказательством механизма 5N2 ( P) служит бимолекулярная кинетика реакции в сочетании, с наличием изотопных эффектов, стереохимических изменений и невозможностью выделения промежуточного продукта. [25]
Эксперимент показывает, что Fe ( III) замедляет реакцию, тогда как Т1 ( 1) не оказывает такого действия. Эти данные также служат доказательством одноэлектронного механизма с образованием Т1 ( П) в качестве промежуточного соединения. Рассмотренная реакция является достаточно общей моделью реакций Т1 ( П1) со способными окисляться ионами переходного металла. [26]
Важнейшая особенность ЛА О С-механизма состоит в том, что в результате реакции азот из амида калия и один из гете-роатомов обмениваются местами. На этом основан наиболее надежный метод доказательства механизма. Если в исходном соединении пометить оба атома азота меткой 15N, то при 100 % - ной реализации ЛА О С-механизма содержание метки в 4-бромо - 6-фенилпиримидине, полученном например, по схеме ( 10), будет вдвое меньше, чем в исходном веществе. Примеров прохождения реакции исключительно по ANRORC-механизму сравнительно немного. При этом содержание метки в гетерокольце продукта замещения оказывается больше 50 % и по нему можно оценить вклад каждого из путей реакции. [27]
В определенных случаях, например при изомеризации а-фенилаллилового эфира ге-нитробензойной кислоты [149, 150] и а-фенил - - метилаллилового эфира к-нитробензойной кислоты [123], атом кислорода исходного сложного эфира становится алкоксильным кислородом его изомера. На первый взгляд это может служить доказательством SNl механизма. Однако, как указывали Уинстейн и Робинсон [61], такие результаты можно объяснить образованием промежуточной внутренней ионной пары, is которой ионы могут вращаться относительно друг друга, если только они смогут преодолеть довольно значительные электростатические силы. [28]
В определенных случаях, например при изомеризации а-фенилаллилового эфира га-нитробензойноы кислоты [149, 150] и а-фенил-у-метилаллилового эфира n - нитробензойной кислоты [123], атом кислорода исходного сложного эфира становится алкоксильным кислородом его изомера. На первый взгляд это может служить доказательством Spji механизма. Однако, как указывали Уинстейн и Робинсон [61], такие результаты можно объяснять образованием промежуточной внутренней ионной пары, в которой ионы могут вращаться относительно друг друга, если только они смогут преодолеть довольно значительные электростатические силы. [29]
Уравнения, полученные на основе рассмотренного выше механизма реакции, проверялись на многих примерах и приводили к ожидаемым результатам. Поэтому соответствие процесса этим уравнениям можно рассматривать как доказательство механизма, полученное методами фотокинетики. Поскольку для сенсибилизированной изомеризации доказан механизм с участием триплетных состояний, то аналогичное протекание несенсибилизированной реакции может служить доказательством триплетного механизма и для последней. [30]
Страницы: 1 2 3 4