Конфигурация - хиральный центр
Cтраница 3
Электронодонорные заместители, а также заместители, вызывающие стерические затруднения, препятствуют реакции. Вальденовское обращение - обращение конфигурации хирального центра, по которому протекает реакция по S - механизму. [31]
Несмотря на то, что RS-систша является единственным точным общим методом описания конфигурации, в номенклатуре углеводов для выражения конфигурации нижнего хирального центра используют обозначения D и L. Обозначение D получает тот из стереоизо-меров, конфигурация нижнего хирального центра которого соответствует конфигурации правовращающего глицеринового альдегида; L-конфигурация моносахарида соответствует конфигурации левовращающего изомера глицеринового альдегида. Эти изомеры первоначально обозначали буквами d и I, указывающими направление вращения. Из-за возможных недоразумений использования d и I следует избегать. [32]
В настоящее время в практике нефтепоисковых исследований для определения степени зрелости нефти и прочих УВ соединений нефти используют коэффициенты, основанные на молекулярных соотношениях биомаркеров - стерановых и гопановых УВ. Эти полициклические УВ в процессе катагенеза претерпевают изменения конфигурации хиральных центров. Эта эпимериза-ция и является той мерой, которая способна оценить степень созревания биоорганических молекул, т.е. переход биоизомеров в геоизомеры. Разными авторами предложены различные коэффициенты. [33]
Что же касается хербертанов, то это метаболиты наземных растений. В высших растениях найдено несколько собственно хербертанов с конфигурацией хирального центра такой же, как у купаранов. [34]
Поскольку не существует простой связи между направлением вращения света и абсолютной конфигурацией, трудно выбрать, какая из альтернативных схем верна. В настоящее время установлено, что все 5ы2 - реакции сопровождаются обращением конфигурации хирального центра, у которого происходит замещение. Этот вывод, сделанный первоначально на основании циклической последовательности реакций, был затем изобретательно подтвержден при исследовании взаимодействия изотопно меченного ( радиоактивного) иодид-иона с оптически чистым 2-иодооктаном. Алкилиодид при этом рацемизуется в результате 5 -замещения нормального иодида на радиоактивный ио-дид-ион. [35]
С точки зрения обшей стратегии, оба эти синтеза построены на последовательном усложнении системы циклов в порядке В - АВ - ABC. При реализации этой схемы необходимо было решить проблемы, связанные с созданием надлежащей конфигурации хиральных центров, возникающих при построении каждого из этих фрагментов. [36]
С точки зрения общей стратегии, оба эти синтеза построены на последовательном усложнении системы циклов в порядке В - АВ - ABC. При реализации этой схемы необходимо было решить проблемы, связанные с созданием надлежащей конфигурации хиральных центров, возникающих при построении каждого из этих фрагментов. [37]
С точки зрения общей стратегии, оба эти синтеза построены на последовательном усложнении системы циклов в порядке В - АВ - ABC. При реализации этой схемы необходимо было решить проблемы, связанные с созданием надлежащей конфигурации хиральных центров, возникающих при построении каждого из этих фрагментов. [38]
Проблема асимметрического синтеза включает как качественный, так и количественный аспекты. Качественно в каждом асимметрическом синтезе образуется продукт, который содержит молекулы с преимущественной R - или - конфигурацией образовавшегося хирального центра. Количественно степень, в которой один изомер преобладает над другим, может сильно варьировать - от малых величин, которые лежат за пределами чувствительности эксперимента, до почти 100 %; последняя величина получается в ферментативных процессах на природных субстратах. Всякое детальное изучение асимметрического синтеза должно состоять в изучении изменения как качественной ( конфигурация продукта), так и количественной ( степень асимметрического синтеза) картины, обусловленной изменением ряда возможных параметров, таких, как температура, растворитель, изменения в природе хирального реагента и изменения строения молекулы субстрата. Слишком часто ограниченные стереохимические результаты служат основой для неоправданных обобщений относительно природы несвязанных взаимодействий в переходном состоянии и его структуры. [39]
Лиль ( 1968) [1 ] нашел, что и эффект Коттона ( при 260 нм) этого производного также положителен при D-конфигурации С-3. Эффект Коттона, обусловленный присутствием многих других гетероциклических группировок в производных моносахаридов, может быть применен для определения конфигурации отдельных хиральных центров: С-2 - бензимидазолов; С-3 - хиноксалинов, озазонов; С-5 - ангидроозазонов и диангидроозазонов. [40]
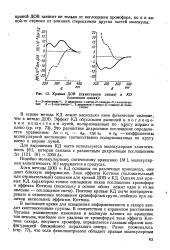 |
Кривые ДОВ ( пунктирная линия и ( сплошная линия. [41] |
В настоящее время для повышения информативности в сахара вводят коттоногенные группы. В соответствии с правилом расстояния Чугаева ( химические изменения в молекуле влияют на вращение тем меньше, чем бол ее они удалены от хромофора) знак эффекта Кот-тона сахара, несущего хромофор, определяется главным образом конфигурацией ближайшего хирального центра. [42]
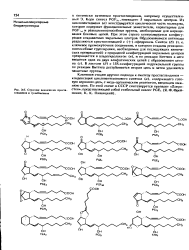 |
Строение важнейших проста-гландинов н тромбоксанов. [43] |
Из циклопеитадиена ( а) конструируется циклическая часть молекулы, которая содержит функциональные заместители, характерные для PGF, , и реакционноспособные группы, необходимые для наращивания боковых цепей. При этом строго контролируется конфигурация создаваемых хиральных центров. Образовавшиеся антиподы разделяются кристаллизацией с () - эфедрином. В лактоне ( д) с lSS - коифигурацией гидроксильной группы по реакции Виттига достраивается вторая цепь и затем удаляются защитные группы. [44]
В малых и средних циклах благодаря сравнительной жесткости С-С - связей колец конформационныв факторы особой роли не играют. В этих случаях существует четкая связь между пространственной ориентацией заместителей и конфигурацией хи-ральных центров. Например: энантиомеры, составляющие ifue - диастереомер 1-метил - 2-этилциклопентана, имеют конфигурацию хиральных центров dl и Id, а энантиомеры трянс-1 - метил-2 - этилциклопентана имеют dd - и И-конфи-гурации. Благодаря конформационной жесткости молекулы термины цис и транс имеют здесь явно выраженный конфигурационный характер. Однако уже в восьмичленном цикле подвижность С-С - связей в кольце такова [30], что вици-нальные заместители могут быть повернуты ( в конформационном смысле) так, что ifuc - изомер превратится в транс-изомер, и наоборот. Понятно, что при этом конфигурация хиральных центров не изменится. В то же время, чтобы однозначно связать эту конфигурацию с пространственной ориентацией заместителей, необходимо уже уточнить конформацию восьмичленного кольца рассматриваемой молекулы. То же самое имеет место и в алканах, где основная углеродная цепь обладает еще большой подвижностью. Поэтому чтобы в данном случае связать пространственную ориентацию заместителей с конфигурацией хиральных центров диастереомеров, также необходимо однозначное определение того конформационного состояния молекулы, в котором эта ориентация будет рассматриваться. Иначе говоря, молекуле алканов необходимо придать хотя бы мысленно конформационную жесткость. [45]
Страницы: 1 2 3 4