Равновесная конфигурация - молекула
Cтраница 3
 |
Кривые потенциальной энергии основного состояния. [31] |
За время колебательного периода ( - 10 - 13 с) устанавливается новая равновесная конфигурация молекулы. [32]
Эти смещения можно представить наглядно, если совместить рис. 7.5, изображающий равновесную конфигурацию молекулы воды с жестко связанными с ней осями ( х, у, z), с рис. 7.7 таким образом, чтобы оси ( х, у, z) равновесной конфигурации совпадали с осями ( х, у, z) искаженной молекулы. [33]
Рг ( уад-дроекции оператора дипольного момента на декартовы оси коорди-яат, связанные с равновесной конфигурацией молекулы. [34]
При расчете из-за сходства ИК-спектров конденсата и озона использовались геометрические параметры и силовые постоянные равновесной конфигурации молекулы озона. [35]
Если молекула имеет единственную равновесную конфигурацию ядер, то мы можем определить точечную группу симмег-рии равновесной конфигурации молекулы. Например, ядра молекулы CH3F в равновесной конфигурации основного электронного состояния образуют структуру с точечной группой симметрии C3v: С - F-связь совпадает с осью вращения 3-го порядка, плоскость Н - С - F - плоскостью отражения. [36]
NN обозначены все пары тождественных ядер, расположенных симметрично относительно центра масс ядер, в равновесной конфигурации молекулы. [37]
Задача решается в предположении, что все ядра неподвижны и фиксированы в положениях, соответствующих заданной равновесной конфигурации молекулы. [38]
Для нелинейных многоатомных молекул классификация МО ведется по отношению к операциям симметрии, характерным для данной равновесной конфигурации молекулы: а - симметричные типы орбита-лей, Ь - антисимметричные, е - - дважды вырожденные ( от немецкого слова entartet), t - трижды вырожденные. Эти многоцентровые МО приближенно описываются как линейные комбинации атомных орбиталей всех атомов. В этой картине нет места, казалось бы, для локализованных двухцентровых связей, хорошо описывающих для многих молекул и направленность орбиталей, и целочисленность валентности, и аддитивность свойств. Однако, как показал Леннард-Джонс, для многоатомной молекулы волновая функция, построенная из делокали-зованных многоцентровых молекулярных орбиталей, в определенных случаях может быть математически преобразована в функцию, построенную из двухцентровых, локализованных молекулярных орбиталей. А это значит, что хотя электроны в такой молекуле делокализованы, общее распределение электронной плотности такое или почти такое, как если бы в ней существовали локализованные двухцентровые связи. Поэтому для таких молекул можно использовать наглядное представление о локализованных связях, вводя для них двухцентровые МО. Это очень удобно, так как позволяет рассматривать молекулы в привычных химику образах отдельных двухцентровых связей. [39]
 |
Система электронно-колебательных полос. а - общий случай. б - поперечная серия. в - продольная серия. [40] |
Для нелинейных многоатомных молекул классификация электронных состояний по типам симметрии может быть произведена в соответствии с принадлежностью равновесной конфигурации молекулы к определенной точечной группе конечного порядка ( см. табл.) и аналогична классификации колебат. Нормальные колебания молекул), при этом необходимо, однако, учитывать, что, согласно Яна - Теллера теореме, вырожденные электронные состояния нелинейных молекул неустойчивы, о чем упоминалось выше. Правила отбора для переходов между электронными состояниями также аналогичны правилам перехода между колебат. [41]
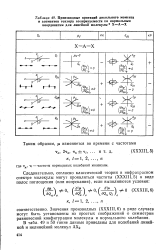 |
Производные проекций дипольного момента. [42] |
Значения производных ( XXXIII, 6) в ряде случаев могут быть установлены из простых соображений о симметрии равновесной конфигурации молекулы и нормального колебания. [43]
Если в молекуле имеется несколько ядер определенной индивидуальности, переходящих друг в друга при операциях симметрии, допускаемых равновесной конфигурацией молекулы, то постоянные экранирования о для таких ядер одинаковы. [44]
Путем суммирования всех неплоскостных и торсионных членов полная потенциальная энергия молекулы V может быть выражена в значениях смещений гг. Равновесной конфигурацией молекулы будет тогда набор значений гт, минимизирующий V, при условии, чтобы расстояния между атомами в области перекрывания были равны наблюдаемым. Этот процесс минимизации приводит к системе уравнений, из которых могут быть найдены как смещения, так и энергии. Удивительно, что такая простая теория оказывается в состоянии дать удовлетворительные результаты. [45]
Страницы: 1 2 3 4