Конформация - белок
Cтраница 1
Конформация белка в значительной мере определяет его химические, физико-химические и биологические свойства. Если ее нарушить, то это приводит к изменению и даже утрате некоторых свойств нативного протеина. Изменившийся продукт обычно называют денатурированным белком. Термин нативный не всегда означает, что состояние очищенного протеина идентично тому, в котором он находится в живой клетке. Даже при самом осторожном выделении неизбежно происходит разрыв слабых связей, которые в клетке соединяют молекулу белка с молекулами иных типов. Высокоочищенные белки могут далеко не полностью соответствовать тем, которые действуют в организме. [1]
Конформация белка стабилизирует центры связывания меди. Тиоловые группы вряд ли могут быть единственными лигандами. Наиболее вероятным лигандом в этом отношении является имидазольный остаток гистидина. [2]
Денатурация, нарушая исходную конформацию белка, освобождает экранированные группы и повышает его реакционную способность. Впервые это было обнаружено для SH-групп яичного альбумина. Оказалось, что денатурация, вызванная тепловой обработкой, действием соляной кислоты, спирта и раствором мочевины, а также ультрафиолетовой радиацией, приводит к выявлению SH-групп, дающих положительную нитропруссидную реакцию. Несколько позже аналогичными приемами была обнаружена экранизация дисульфидных связей, фенольной ОН-груп-пы тирозина и индольной группы триптофана. [3]
Современный уровень знания деталей конформации белков основан почти исключительно на результатах исследования кристаллов белков методом дифракции рентгеновских лучей. [4]
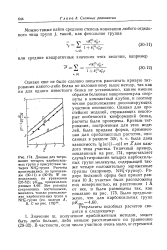
Очень чувствительным методом исследования конформаций белков и полипептидов является спектрополяриметрия. Характер оптического вращения белков в неупорядоченной конформаций определяется прежде всего аминокислотным составом, причем кривые дисперсии оптического вращения имеют плавный характер. [5]
В ходе развития клетки конформации хромосомных белков и их ДНК-комплексов изменяются, и геном испытывает функциональные изменения, становясь более или менее доступным действию регуляторных белков цитоплазмы. По-видимому, главная роль гистонов состоит именно в регуляции структуры хромосом, но не в регуляции дифференцированной транскрипции генов в клетках разного типа. В то же время установлены изменения состава и тонкой структуры хромосомных белков на разных стадиях развития клеток и их дифференцировки. [6]
Первостепенное значение имеет выяснение конформации натив-ного белка, которая определяет специфичность биологического действия. [7]
Атомы многих металлов также стабилизируют пространственную конформацию ферментных и иных белков. Таким действием обладают катионы Са, Zn, Mn, Mg, Co, Cn, Fe 2, иногда Ва и также трехзарядные катионы. Они обеспечивают сохранение третичной и ( или) четвертичной структуры ферментов. Особенно часто встречается стабилизирующее действие иона кальция, который защищает конформацию а-амилазы, предохраняет от денатурации ( и автолиза) трипсин, защищает лизоцим, бактериальные и грибные протеиназы, некоторые пептидазы. Металл, по-видимому, может стабилизировать фермент двумя путями: входя в состав его активного центра ( у истинных метал-лоэнзимов) или присоединяясь к различным иным участкам на поверхности белковой частицы. При стабилизации апоферментов, например ионами Са, вероятно образуются клешневидные связи между металлом и СОО-группами. [8]
Наличие лиганда не обязательно приводит к существенно иной конформации свернутого белка, но способствует стабилизации его нативной формы. На основании опытов по водородному обмену [415], а также с помощью кривых денатурации мочевиной [461] апомиоглобина, глобулярного белка с А0общ 9 ккал / моль, установлено, что этот белок должен быть на 4 ккал / моль менее стабилен, чем миоглобин. Противоположным примером является цитохром с, присутствие в котором ковалентно связанной группы тема абсолютно необходимо для стабильности белковой структуры. [9]
Однако для простейших моделей, отражающих некоторые особенности конформаций белка, расчеты были проведены. [11]
 |
Строение поперечнополосатой мышцы. [12] |
Взаимодействие между ионами кальция и тропонином приводит к изменению конформации белка, прекращающему его ингибирующее действие, и, таким образом, включает механизм сокращения мышцы. [13]
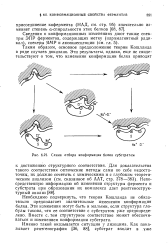 |
Схема отбора конформации белка субстратом. [14] |
Необходимо подчеркнуть, что теория Кошланда не обязательно предполагает значительные изменения конформации белка. Эти изменения могут быть и малыми, если структура глобулы такова, что ее соответствие с субстратом уже предопределено. [15]
Страницы: 1 2 3 4