Концентрация - ион - ртуть
Cтраница 2
При изменении концентрации хлористого калия меняется и концентрация ионов ртути, а в связи с этим и потенциал электрода. [16]
Каломель - труднорастворимое соединение, следовательно, концентрация ионов ртути в растворе очень мала, а в присутствии хлористого калия еще больше понижается, так как у обоих солей имеется общий ион С1 -, и остается постоянной при сохранении концентрации КС1 неизменной. [17]
Из соотношений ( 17, 18) видно, что при концентрации ионов ртути в растворе 0 05 мкг / см3 электровыделение ртути на графике определяется ростом зародышей. [18]
В системе ртуть - нитрат ртути ( I) десятикратное изменение концентрации ионов ртути и, следовательно, примерно такое же изменение активности раствора приводят к понижению потенциала системы на 0 029 в. [19]
 |
Каломельный электрод. [20] |
Скачок потенциала в каломельном электроде образуется на границе ртуть-каломель и зависит от концентрации ионов ртути в растворе каломели. [21]
Каломель Hg2Cl2 - соль, трудно растворимая в воде, следовательно, концентрация ионов ртути Hg2 B растворе очень мала. [22]
Потенциал каломельного электрода зависит от концентрации ионов ртути в пасте каломели, а концентрация ионов ртути в свою очередь зависит от концентрации ионов хлора. [23]
Каломель Hg2Cl2 - соль, трудно раствор ff ая в воде, следовательно, концентрация ионов ртути Hg2 B растворе очень мала. [24]
Эти соображения показывают нам, между прочим, что протекшее количество электричества изменяет не только концентрацию ионов ртути блаюдаря осаждению или растворению, но также и заряд электрода. Для последнего количества электричества закон Фарадея, следовательно, не имеет силы; вследствие его незначительности, что явствует из данных, приведенных на стр. [25]
Падение капель ртути в жидкости, содержащей ионы ртути, помимо разделения электрических зарядов, должно вызвать изменение концентрации ионов ртути; при положительном заряде капель последняя будет увеличиваться в верхней части сто: ба и уменьшаться в нижней. Это должно привести к возникновению шкоторой, обратной по знаку седиментационному потенциалу, рази сти потенциалов между ртутными электродами 1 -го рода, находящимися в соприкосновении с раствором. В отличие от седиментационного потенциала эта разность потенциалов не исчезает с прекращением падения капель через раствор, а сохраняется до выравнивания разности концентраций в столбе жидкости диффузией. [26]
Меркурирование бензола в уксусной кислоте является реакцией второго порядка, первого порядка по ароматическому углеводороду и первого порядка по концентрации иона ртути. Реакция заметно катализируется хлорной кислотой и перхлоратом натрия, ион хлора ее замедляет. [27]
Так как ПР при постоянной температуре есть величина постоянная, увеличение концентрации иона хлора может оказать существенное влияние на концентрацию ионов ртути, а следовательно, и на потенциал каломельного электрода. [28]
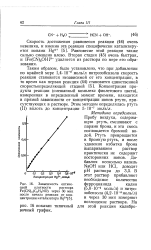 |
Зависимость оптической плотности раствора Fe ( CN5 ( CeH6NO через 30 мин после начала реакции от концентрации катализатора Н § 2. [29] |
Концентрация продукта реакции ( смешанный комплекс фиолетового цвета), измеренная в определенный момент времени, находится в прямой зависимости от концентрации ионов ртути, присутствующих в растворе. [30]
Страницы: 1 2 3 4