Концентрация - ион - серебро
Cтраница 2
Coli от концентрации ионов серебра ( рис. 11) показывает, что исследуемые микробные клетки имеют отрицательный электрический потенциал. Величина его при инактивации клеток кипячением существенно не меняется. [16]
При измерениях концентрации ионов серебра, ртути и галогенидов нельзя пользоваться насыщенным солевым мостиком, так как ионы хлора будут диффундировать в раствор, подлежащий измерению. Применяют специальные приспособления для предотвращения диффузии соли в par створ. При нотенциометрическом титровании с серебряным или ртутным электродом, где диффузионный потенциал не имеет особенно существенного значения, можно уш греблять солевые мостики из нитрата калия, сульфата калия, или нитрата аммония ( в виде их геля в 3-про. [17]
Например, если концентрация ионов серебра равна всего 10 30 моль - л i, потенциал серебряного электрода оказывается равным - 1 0 В, что представляет собой вполне измеримую величину. [18]
За эквивалентной точкой концентрация ионов серебра зависит от избытка осадителя и вычисляется также из ПР. [19]
Пусть после прибавления концентрация ионов серебра будет с; значение это соответствует также и концентрации ионов хтора, происходящих от диссоциации хлористого серебра. [20]
В эквивалентной точке концентрация ионов серебра определяется из следующего рассуждения. [21]
В конце концов концентрация иона серебра ( возрастает настолько, что вызовет осаждение второго иона. Какова будет концентрация первого иона, когда второй ион начнет осаждаться. [22]
Следовательно, произведение концентраций ионов серебра и иода в растворе значительно больше, чем произведение растворимости иодида серебра Agl. Значит, осадок иодида серебра выпадет и комплекс К [ Ag ( CN) 21 разрушится. [23]
Следовательно, произведение концентраций ионов серебра и иода в растворе значительно больше, чем произведение растворимости иодида серебра Agl. Значит, осадок иодида серебра выпадет и комплекс KlAg ( CN) 2 ] разрушится. [24]
При сопоставлении величин концентраций ионов серебра, доставляемых в раствор из осадка AgCl, и комплексной соли [ Ag ( NH3) 2 ] Cl видно, что она в последнем случае в 1000 раз меньше, чем в первом, и вполне очевидно, что осадок AgCl будет растворяться в аммиаке. [25]
Молекулы аммиака понижают концентрацию ионов серебра в растворе. В результате равновесие реакции растворения сдвигается вправо и растворимость бромида серебра увеличивается. [26]
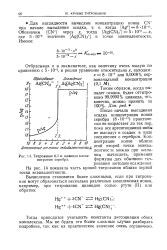 |
Титрование 0 1 н. цианида калия нитратом серебра. [27] |
После начала выпадения осадка концентрация ионов серебра ( 8 - 10-и) практически не возрастает до тех пор, пока все аргентоцианид-ионы не выпадут в осадок в виде соединения с серебром. Концентрации ионов вблизи этой второй точки эквивалентности можно при желании вычислить, применяя формулы для обычного титрования методом осаждения. [28]
В то же время концентрация ионов серебра, доставленных в раствор при диссоциации комплексного иона [ Ag ( NH3) 2 ], может быть легко рассчитана из величины константы нестойкости. [29]
При прибавлении аммиака уменьшается концентрация ионов серебра, так как часть нх расходуется на образование новых ионов и произведение наличных концентраций становится меньше произведения растворимости. [30]
Страницы: 1 2 3 4