Концентрация - ион - серебро
Cтраница 4
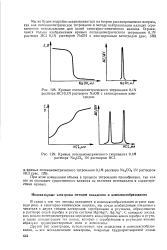 |
Кривые потенциометрического титрования О, IN раствора НС1 О IN раствором NaOH с хингидронным электродом.| Кривые потенциометрического титрования 0 Ш раствора Na2CO3 IN раствором НС1. [46] |
С помощью последних можно потенциометрически определить концентрацию ионов серебра и ртути, а также концентрации тех ионов, которые с серебряными и ртутными ионами образуют труднорастворимые соли и комплексы. [47]
Если надо получить литр воды с концентрацией ионов серебра 10 мг / л, то достаточно вести электролиз в течение 6 мин. [48]
Если теперь прибавить соляной кислоты, то концентрация ионов серебра в растворе уменьшится, потому что осаждается хлористое серебро. Ради простоты, предположим, что объем раствора серебра не изменяется от прибавления соляной кислоты, что мало влияет на результаты. [49]
Если раствор хранят в полиэтиленовом сосуде, концентрация ионов серебра почти не уменьшается в течение месяцев. [50]
Это значение указывает на то, что концентрации иона серебра и хлорид-иона ( равные друг другу в насыщенном водном растворе хлорида серебра) очень малы; это подтверждается низкой растворимостью хлорида - серебра. [51]
Полученное уравнение показывает, что с увеличением концентрации ионов серебра в электролите число ад-атомов, а следовательно, и вероятность образования зародышей при кристаллизации уменьшается. [52]
Обычно ti и миграция не может компенсировать убыли концентрации ионов серебра в результате их разряда. [53]
Обычно tj и миграция не может скомпенсировать убыли концентрации ионов серебра в результате их разряда. [54]
Добавляя 1 N раствора хлорида, мы уменьшим концентрацию ионов серебра, переводя их в осадок. Предположим, что добавлено 5 мл 1 N раствора хлорида, что эквивалентно половине содержания ионов серебра. [55]
Страницы: 1 2 3 4