Концентрация - определяемый ион
Cтраница 2
Прибор позволяет автоматически рассчитывать концентрацию определяемого иона при различных соотношениях объемов анализируемого и стандартного растворов ( в том числе и при введении добавки твердой пробы) и выдает полученную величину непосредственно на дисплее. [16]
В кинетических методах анализа концентрацию определяемого иона ( чаще всего катализатора) определяют по скорости каталитической реакции. Реакция, скорость которой определяется концентрацией катализатора, называется индикаторной. Реакция окисления ализарина перекисью водорода, например, является индикаторной по отношению к ионам кобальта, которые катализируют эту реакцию. Вещества, по изменению концентрации которых определяют скорость реакции, называют индикаторными. Так, ализарин выступает в роли индикаторного вещества в указанной индикаторной реакции на кобальт. В реакции окисления гидрохинона перекисью водорода катализатором являются ионы меди. В результате реакции образуются окрашенные продукты, которые следует считать индикаторными веществами. [17]
В точке эквивалентности, когда концентрация определяемого иона равна нулю, происходит резкий скачок потенциала, регистрируемый чувствительным гальванометром. [18]
Для бинарных электролитов типа АВ концентрация определяемого иона равна [ А ] [ В ] ПР. [19]
Электрод, реагирующий на изменение концентрации определяемого иона в растворе и заменяющий индикатор в условиях обычного титрования, называется индикаторным. Его потенциал определяется по отношению к неполяризуемому электроду, называемому стандартным, потенциал которого в процессе титрования постоянен и служит исключительно для определения потенциала индикаторного электрода. Последний выбирают в зависимости от типа реакций, лежащих в основе титрования, но во всех случаях его потенциал должен устанавливаться мгновенно соответственно концентрации титруемых ионов и не зависеть от наличия посторонних ионов. [20]
Поэтому анализ начинают с повышения концентрации определяемого иона путем выпаривания больших количеств раствора. Между тем повышение концентрации определяемого иона достигается быстро и просто при помощи ионообменных смол. [21]
При потенциометрическом титровании по методу комплексообразования концентрация определяемого иона вычисляется с учетом константы нестойкости образовавшегося комплекса. В этом случае так же, как и при реакции осаждения, происходит резкий скачок потенциала, который позволяет определить эквивалентную точку. [22]
В случае электролиза раствора небольшого объема концентрация определяемого иона меняется значительно. При достаточно большом времени накопления металл может практически полностью перейти из раствора в амальгаму. Обычно эффективность электролиза оценивают по уменьшению предельного тока восстановления определяемого иона. Так, если принять, что при концентрации вещества в растворе - 10 моль / л среднее значение тока для висячей ртутной капли ( - 0 05 см) составляет - 0 5 мкА, то уже после десятиминутного электролиза величина предельного тока становится трудно измеримой с помощью обычных вольтамперо-графов. [23]
Электрод, который реагирует на изменение концентрации определяемого иона в растворе и заменяет собой индикатор при обычном титровании, называется индикаторным электродом. [24]
Уравнение ( 4) позволяет рассчитать концентрацию определяемого иона. [25]
Электрод, по потенциалу которого судят о концентрации определяемых ионов в растворе, называют индикаторным электродом. [26]
Электрод, по потенциалу которого судят о концентрации определяемых ионов, называется индикаторным электродом. Значение величины индикаторного электрода находят, сравнивая с величиной потенциала другого электрода, который принято называть электродом сравнения. Потенциал электрода сравнения не должен изменяться от изменения концентрации определяемых ионов. [28]
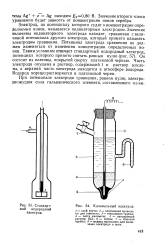 |
Стандартный водородный электрод.| Каломельный электрод. [29] |
Электрод, по потенциалу которого судят о концентрации определяемых ионов, называется индикаторным электродом. Значение величины индикаторного электрода находят, сравнивая с величиной потенциала другого электрода, который принято называть электродом сравнения. Потенциал электрода сравнения не должен изменяться от изменения концентрации определяемых ионов. Он состоит из платины, покрытой сверху платиновой чернью. Водород хорошо растворяется в платиновой черни. [30]
Страницы: 1 2 3 4
