Равновесная концентрация - аммиак
Cтраница 1
 |
Равновесная концентрация NH3 ( в мол. % в смеси азота н водорода стехиометрического состава. [1] |
Равновесные концентрации аммиака при t 325 - 500 С и Р 10 - 1000 am в смеси азота и водорода стехиометрического состава были определены экспериментально Ларсоном и Доджем. [2]
Равновесная концентрация аммиака Zp ( в объемн. [3]
Таким образом, равновесные концентрации аммиака в случаях I и II не могут быть одинаковыми. [4]
В каких соотношениях находятся равновесные концентрации аммиака для этих случаев. [5]
Там же имеются таблицы равновесной концентрации аммиака. [6]
При разбавлении азото-водородной смеси инертным газом равновесная концентрация аммиака уменьшается в большей степени, чем соответствовало бы снижению парциальных давлений азота и водорода. [7]
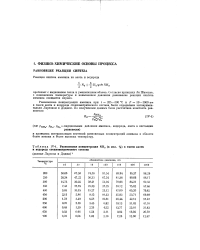
Данные этой таблицы показывают резкое снижение равновесной концентрации аммиака при увеличении температуры синтеза. Однако применение высоких давлений ( до 1000 атм), приводящих к весьма значительному росту равновесных концентраций аммиака, позволяет практически осуществлять синтез на катализаторах при 400 - 550 С; эти условия обеспечивают ( при достаточно больших объемных скоростях) выход аммиака, равный 30 - 60 % теоретического. Этот катализатор и был применен в указанных выше исследованиях равновесия синтеза аммиака. Повышение давления при синтезе выше 1000 атм обусловливает дальнейший значительный рост равновесной концентрации аммиака. [8]
Возможно также определить в растворе комплекса равновесную концентрацию аммиака ( с помощью стеклянного электрода) и таким образом прийти к вычислению величины К. [9]
В табл. 41 приведены экспериментальные данные о равновесных концентрациях аммиака при давлениях выше 1000 ат. [10]
При температуре, состгветствующей максимальной активности катализатора, высокая равновесная концентрация аммиака: достигается при давлении 100 МПа и более. Однако изготовление оборудования па такое давление очень сложно, оно отличается высокой стоимостью и большим расходом энергии на сжатие азотоводородной смеси до 100 МПа. В настоящее время считается экономичным давление процесса, равное 30 МПа, При приближении к равновесию скорость реакции резко замедляется, поэтому в промышленных условиях содержание аммиака достигнет не более 50 % равновесного. При этом пребывание газа в катализаторной зоне измеряется секундами. [11]
При разбавлении азотоводородной смеси инертными газами ( метаном и аргоном) равновесная концентрация аммиака также уменьшается. Тониоло [4] или более точно по - уравнению Гиллеспая - Битти. [12]
При низком давлении в конденсаторе 14 ( см. рис. 11) равновесная концентрация аммиака в газовой фазе рассчитывается по закону Дальтона: а PHnNHj ( Т) / Я, где Риикн, - давление насыщенных паров аммиака. Структурный анализ системы уравнений баланса конденсатора аммиака показал, что ее решение может быть сведено к итерациям по одной переменной, например, количеству g конденсата аммиака. [13]
Повышение давления при синтезе выше 1000 атм обусловливает дальнейший значительный рост равновесной концентрации аммиака. [14]
 |
Зависимость равновесной концентрации аммиака ( в % от состава исходной смеси 7. [15] |
Страницы: 1 2 3 4