Равновесная концентрация - аммиак
Cтраница 2
Влияние инертных газов на равновесную концентрацию NH3 - При разбавлении азото-водородной смеси инертными газами равновесная концентрация аммиака уменьшается в большей степени, чем соответствовало бы снижению парциальных давлений азота и водорода. [16]
Высокой скорости реакции благоприятствуют высокие температуры и давление, но высокая температура означает более низкое значение равновесной концентрации аммиака и, следовательно, меньшую движущую силу. Поэтому скорость реакции возрастает с увеличением температуры, но достигает максимального значения и затем падает, поскольку приближается к равновесию. Вследствие этого оптимальный выход при заданном давлении получается в виде профиля, падающего вдоль слоя катализатора при возрастании температуры и содержания аммиака. В промышленных условиях максимальная скорость реакции получается при температуре на 70 С ниже равновесной. Таким образом, уравнение, описывающее скорость синтеза аммиака, должно учитывать температуру, давление, состав газа и равновесный состав. [17]
Для процесса синтеза аммиака в условиях протекания процесса в переходных и знутрядиффузионных областях внутри гранулы создаются участки с равновесными концентрациями аммиака, которые не принимают участия в катализе, В этом случае приготовление зерен контакта меньшего размера, как указано в / 23 /, дробление крупных зерен на мелкие / Зо / приведет к увеличению доступности внутренних участков гранулы для катализа, внутреннее диффузионное затруднение уменьшается, за счет чего увеличится удельная производительность контакта. Для полного использования потенциальных возможностей катализатора размер зерен целесообразно уменьшать до дочти полного снятия внутренних диффузионных затруднений, что проявится в прекращении дальнейшего увеличения удельной нроазво - дителыюств с уменьшением размера зерен. [18]
Для процесса синтеза аммиака в условиях протекания процесса в переходных и внутридиффузионннх областях внутри гранулы создаются участки с равновесными концентрациями аммиака, которые не принимают участия в катализе. В этом случае приготовление зерен контакта меньшего размера, как указано в & /, дробление крупных зерен на мелкие § 0 / приведет к увеличению доступности внутренних участков гранулы для катализа, внутреннее диффузионное затруднение уменьшается, за счет чего увеличится удельная производительность контакта. Для полного использования потенциальных возможностей катализатора размер зерен целесообразно уменьшать до почти полного снятия внутренних диффузионных затруднений, что проявится в прекращении дальнейшего увеличения удельной произво - - дительности с уменьшением размера зерен. [19]
 |
Генератор с ректификационной колонной. [20] |
На i - - диаграмме изотермы в области влажного пара не показаны; их проводят в соответствии с равновесными концентрациями аммиака в жидкой фазе и парах; например, на рис. 9 - 16 точке 1 концентрации аммиака в жидкой фазе соответствует точка 2 концентрации аммиака в парах, которая определяется как пересечение изотермы с данной изобарой. Линия 1 - 2 соответствует изотерме влажного пара. В пределах равных изобар для жидкой и паровой фаз изотермы образуют сетку прямых линий с различными уклонами. Для других значений изобар они могут иметь другие уклоны и пересекаться с первыми изотермами; вследствие этого сетки изотерм влажного пара на i - - диаграмму не наносятся. [21]
Си ( МНз) 1, Cu ( NH3) и Cu ( NH3) - в растворе, в котором равновесные концентрации аммиака и иона Си2 равны 2 50 - 10 - 3 F и 1 50 - Ю-4 М соответственно. [22]
Изучение равновесия системы дает возможность установить оптимальные условия ведения процесса, а сравнение выхода с равновесным позволяет оценить эффективность процесса синтеза. Равновесная концентрация аммиака входит в кинетическое уравнение ( стр. [23]
Зависимость Кр от температуры выражается изобарой реакции Вант-Гоффа ( см. стр. В таблице также приведены равновесные концентрации аммиака при различных давлениях при условии, если исходная смесь. [24]
 |
Равновесные концентрации аммиака при различных условиях. [25] |
Они показывают, что равновесная концентрация аммиака увеличивается с давлением. Таким образом, синтез аммиака следует проводить при возможно более высоком давлении. Как известно, это требование соблюдается в методах синтеза, применяющихся в промышленности, где давления достигают 1000 атм. С другой стороны, повышение температуры уменьшает равновесную концентрацию ( выход) аммиака. Следовательно, его синтез надлежало бы проводить при возможно более низкой температуре. Эту вторую рекомендацию, вытекающую из изучения тепловых явлений и термических свойств, не удается использовать в полной мере. Фактор времени учитывается в другом разделе физической химии - химической кинетике. Она подсказывает, что скорость химической реакции очень быстро уменьшается с понижением температуры. Поэтому может оказаться, что при какой-то температуре хороший выход может быть достигнут за слишком продолжительное время, скажем за миллиард лет. С другой стороны, согласно данным кинетики скорость реакции можно увеличить применением катализаторов. [26]
С повышением температуры константа скорости синтеза аммиака растет. Но скорость синтеза зависит также от равновесной концентрации аммиака в газе, которая с повышением температуры уменьшается. [27]
По полученным данным была проведена экстраполяция значений равновесных концентраций аммиака в область более низких и более высоких температур. Данные табл. 6 показывают резкое снижение равновесной концентрации аммиака при увеличении температуры синтеза. [28]
По полученным данным была проведена экстраполяция значений равновесных концентраций аммиака в области более низких и более высоких температур. Данные этой таблицы показывают резкое снижение равновесной концентрации аммиака при увеличении температуры синтеза. Однако применение высоких давлений ( до 1000 атм), приводящих к весьма значительному росту равновесных концентраций аммиака, позволяет практически осуществлять синтез на катализаторах при 400 - 550; эти условия обеспечивают ( при достаточно больших объемных скоростях) выход аммиака, равный 30 - 60 % теоретического. [29]
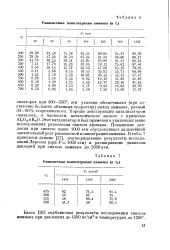 |
Равновесные концентрации аммиака ( в %.| Равновесные концентрации аммиака ( в %. [30] |
Страницы: 1 2 3 4