Равновесная концентрация - аммиак
Cтраница 4
Азотоводородная смесь, получаемая конверсией углеводородов и газификацией твердого топлива, содержит инертные для синтеза аммиака компоненты - аргон и метан. Аргон вносится с атмосферным воздухом, а остаточное содержание метана определяется параметрами процессов конверсии, газификации и метанирования. В цикле синтеза аммиака неизбежно постепенное накопление аргона и метана, снижающих равновесную концентрацию аммиака в значительно большей степени, чем вызванное ими уменьшение парциальных давлений водорода и азота. Поэтому содержание аргона и метана в циркулирующей смеси строго регламентируется и поддерживается на определенном уровне путем постоянной продувки части газов. [46]
Данные этой таблицы показывают резкое снижение равновесной концентрации аммиака при увеличении температуры синтеза. Однако применение высоких давлений ( до 1000 атм), приводящих к весьма значительному росту равновесных концентраций аммиака, позволяет практически осуществлять синтез на катализаторах при 400 - 550 С; эти условия обеспечивают ( при достаточно больших объемных скоростях) выход аммиака, равный 30 - 60 % теоретического. Этот катализатор и был применен в указанных выше исследованиях равновесия синтеза аммиака. Повышение давления при синтезе выше 1000 атм обусловливает дальнейший значительный рост равновесной концентрации аммиака. [47]
К сожалению, измерение скорости соединения азота и водорода в аммиак связано с большими трудностями. Такие определения практически невыполнимы при давлении в 1 ат, так как равновесная концентрация аммиака при этом давлении равна лишь нескольким десятым процента. При более высоких давлениях равновесие более благоприятно; однако при этом выделяется много тепла, вызывающего значительный температурный градиент в самом катализаторе. Поэтому до настоящего времени не опубликовано никаких кинетических измерений, которые устанавливали. [48]
По полученным данным была проведена экстраполяция значений равновесных концентраций аммиака в области более низких и более высоких температур. Данные этой таблицы показывают резкое снижение равновесной концентрации аммиака при увеличении температуры синтеза. Однако применение высоких давлений ( до 1000 атм), приводящих к весьма значительному росту равновесных концентраций аммиака, позволяет практически осуществлять синтез на катализаторах при 400 - 550; эти условия обеспечивают ( при достаточно больших объемных скоростях) выход аммиака, равный 30 - 60 % теоретического. [49]
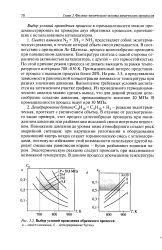 |
Выбор условий проведения обратимого процесса. [50] |
Синтез аммиака N2 ЗН2 NH3 представляет собой экзотермическую реакцию, в течение которой объем смеси уменьшается. В соответствии с принципом Ле-Шателье, процесс целесообразно проводить при повышенном давлении. Температура синтеза с одной стороны ограничена активностью катализатора, с другой - его термостойкостью. По этой причине режим процесса не должен выходить за рамки температурного интервала 700 - 830 К. На рис. 3.5, а представлены зависимости равновесной концентрации аммиака от температуры при разных значениях давления. Выполнение требуемых условий достигается на затемненном участке графика. [51]
Страницы: 1 2 3 4