Равновесная концентрация - продукт
Cтраница 1
Равновесные концентрации продуктов в присутствии А1С13, получающихся при изомеризации этилбензола, приведены в табл. 59 ( в мол. Из данных таблицы видна тенденция к образованию мета-изомера. [1]
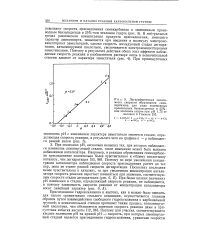
Рассмотрим зависимость равновесных концентраций продуктов сложных реакций от давления. [2]
Штриховыми линиями обозначены равновесные концентрации продуктов. Как видно из рис. 44 и 45, в первой половине змеевика к имеет совершенно другие значения, чем Хр, и соответственно сильно различаются действительный и равновесный составы. Значительная степень приближения к равновесию наблюдается только в конце реактора. [3]
 |
Логарифмическая зависимость скорости образования семи-карбазона для ряда замещенных производных бензальдегида в 25 % - ном этиловом спирте при рН 1 75 от величин ст Гаммета. [4] |
В нейтральных средах равновесная концентрация продукта присоединения, имеющего характер аминоспирта, повышается при введении в молекулу электроно-акцепторных заместителей, однако скорость последующей стадии дегидратации, катализируемой кислотами, увеличивается электроноакцепторными заместителями. [5]
В табл. 20 приведены равновесные концентрации продуктов пиролиза этана и пропана в молярных и весовых процентах. В табл. 21 показаны равновесные концентрации продуктов пиролиза этана при различных давлениях. [6]
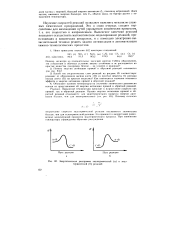 |
Энергетическая диаграмма экзотермической ( а и эндотермической ( б реакций. [7] |
Это приводит к возрастанию равновесных концентраций продуктов эндотермического процесса. При понижении температуры справедливы обратные рассуждения. [8]
Это должно привести к уменьшению равновесной концентрации продукта дегидрогенизации с ростом давления и тем самым значительно понизить скорость дальнейших стадий изомеризации. [9]
Из последнего выражения ясно, что произведение равновесных концентраций продуктов реакции в данном случае в 400 000 раз больше произведения равновесных концентраций исходных веществ. Очевидно, что - в случаях, когда константа равновесия мала, малыми будут и равновесные концентрации продуктов; в таких случаях принимают за первую неизвестную одну из них. В каждом из этих двух случаев используются особые приемы обозначения равновесных концентраций компонентов равновесия; для ознакомления с этими приемами рассмотрим два примера. [10]
 |
Значения - щ. г2 для данных 9. [11] |
Отношение ( 14) является частным от деления произведения равновесных концентраций продуктов реакции на квадрат концентрации исходного вещества. [12]
Ле-Шателье, с повышением температуры равновесие ее сдвигается вправо и равновесные концентрации продуктов возрастают. [13]
Из уравнения протолиза слабой кислоты НА следует, что значения равновесных концентраций продуктов А - и Н3О равны между собой. Предполагая протекание реакции протолиза в малой степени ( что подтверждается расчетом, см. разд. Отсюда по заданным значениям Кк и снд рассчитывают концентрации продуктов реакции протолиза и рН раствора. Значения Кк при 25 С приведены в табл. 7 Приложения. [14]
Для обратимой гомогенной реакции константа равновесия записывается как отношение произведения равновесных концентраций продуктов реакции в степенях, соответствующих их сте-хиометрическим коэффициентам, к произведению равновесных концентраций исходных веществ также в соответствующих степенях. [15]
Страницы: 1 2 3 4