Равновесная концентрация - продукт
Cтраница 2
В заключение этой главы отметим, что давление существенно влияет на равновесные концентрации продуктов сложных, в частности параллельных и параллельно-последовательных, реакций в жидкой фазе, сопровождающихся различными изменениями объема. Этот вопрос будет специально рассмотрен в третьей части книги. [16]
Присутствие инертного компонента или избытка одного реагирующего вещества всегда вызывает понижение равновесных концентраций продуктов в равновесной реакционной смеси. [17]
Если суммарный процесс образования альдолей из альдегидов термодинамически обычно выгоден, то равновесная концентрация продуктов соответствующих реакций в случае кетоноа невелика, и даже в случае ацетона, судя по имеющимся данным, равновесная концентрация XXXII составляет всего лишь несколько процентов. [18]
Если суммарный процесс образования альдолей из альдегидов термодинамически обычно выгоден, то равновесная концентрация продуктов соответствующих реакций в случае кетонов невелика, и даже в случае ацетона, судя по имеющимся данным, равновесная концентрация XXXII составляет всего лишь несколько процентов. [19]
В ( г.): : АВ ( г.) можно увеличить равновесную концентрацию продукта реакции АВ, если ДЯ реакции отрицательно: а) введением в систему катализатора; б) повышением температуры; в) понижением температуры; г) введением в реакционный сосуд дополнительного количества вещества В. [20]
Таким образом, состояние химического равновесия при любой постоянной температуре характеризуется определенным постоянным соотношением равновесных концентраций продуктов реакции и исходных веществ. Существенно, что постоянным сохраняется именно определенное соотношение между равновесными концентрациями реагентов, хотя сами величины равновесных концентраций продуктов реакции и исходных веществ могут быть различными, что зависит от количеств реагентов, введенных в систему. [21]
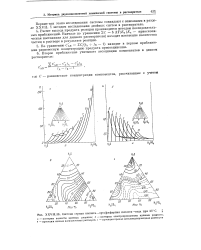 |
Система серная кислота-ортофосфорная кислота-вода при 25 С ]. [22] |
С / ( / л / в - 1) находят в первом приближении равновесную концентрацию продукта присоединения. [23]
Применение законов химической термодинамики дает возможность определить вероятность протекания реакции, максимальную степень превращения и равновесную концентрацию продуктов. [24]
Итак, термодинамический анализ позволяет выяснить направление обратимой реакции при различных условиях, дает возможность подсчитать теоретические равновесные концентрации продуктов реакции, исходя из константы равновесия. Однако для практического осуществления реакции одной ее термодинамической вероятности недостаточно. [25]
Первые три реакции, представленные в табл. 6.3, протекают очень быстро, в результате чего достигаются равновесные концентрации продуктов. При этом концентрация олефинов довольно мала, так как их образование термодинамически невыгодно. Однако олефины образуются на промежуточной стадии реакции изомеризации парафинов. Скорость реакции изомеризации пятичленных алкилнафтенов в шести-членные в десять раз меньше, благодаря дегидрированию, изомеризации до шестичленных циклопарафинов и последующего быстрого их дегидрирования до ароматических. Комбинацию реакций изомеризации и дегидрирования называют дегидроизомеризацией. [26]
Знание величины константы химического равновесия позволяет производить важные расчеты: по известным концентрациям взятых веществ можно вычислить равновесные концентрации продуктов реакции и таким образом судить об эффективности процесса при данных условиях. [27]
В реакциях распада, в отсутствие сольватационных эффектов и иных взаимодействий с растворителем, давление обычно уменьшает равновесные концентрации продуктов реакции. Однако установление самого факта отсутствия влияния растворителя иногда представляет нелегкую задачу. Реакция эта сопровождается увеличением объема; с повышением давления равновесие смещалось в сторону N204: при 1500 атм константа равновесия была приблизительно в четыре раза меньше, чем при атмосферном давлении. Однако оказалось, что находимое по этим данным изменение объема при реакции ( Ду 23 см3 / молъ) почти в десять раз превышает значение этой величины, которое можно вычислить на основании имеющихся сведений о длинах связей в N204 и N02 и ван-дер-ваальсовых радиусов атомов. [28]
Знание величины константы химического равновесия позволяет производить очень важные расчеты: по известным концентрациям взятых веществ можно вычислить равновесные концентрации продуктов реакции и, таким образом, судить об эффективности процесса при данных-условиях. [29]
Знание размера константы химического равновесия позволяет производить очень важные расчеты: по известным концентрациям взятых веществ можно вычислить равновесные концентрации продуктов реакции и, таким образом, судить об эффективности процесса при данных условиях. [30]
Страницы: 1 2 3 4