Коррозия - цинк
Cтраница 2
При коррозии цинка обнажение примесей, которые существуют в цинке в качестве второй фазы, является менее важным фактором. Ни контакт с массивным свинцом, ни сплавление со свинцом5 не является эффективным в отношении увеличения скорости коррозии в кислоте. Губчатые металлы стимулируют коррозию значительно сильнее. Автор считает, что именно обратно осажденные металлические примеси имеют наибольшее значение в образовании точек, на которых происходит выделение водорода. [16]
При коррозии цинка в дистиллированной воде гидроокис-ная пленка хорошо защищает поверхность металла до 50 С; примерно при 60 С металл начинает депассивироваться, а в интервале от 90 до 100 С скорость коррозии снова резко уменьшается вследствие наступления нового устойчивого пассивного состояния. [17]
Скорость коррозии цинка в дистиллированной воде составляет 2 - 2 2 г / м2 - 24 ч; при длительной эксплуатации она уменьшается почти наполовину. При повышении температуры дистиллированной воды до 50 С скорость коррозии растет незначительно, а после 50 С быстро возрастает, достигая максимума примерно при 70 С, и в интервале температур 70 - 100 С уменьшается. [18]
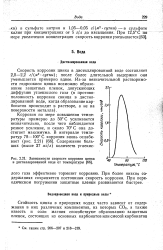 |
Зависимости скорости коррозии цинка в дистиллированной воде от температуры. [19] |
Скорость коррозии цинка в дистиллированной воде составляет 2 0 - 2 2 г / ( м2 сутки); после более длительной выдержки она уменьшается примерно вдвое. [20]
Продукты коррозии цинка малорастворимы и поэтому образуют на поверхности покрытия своеобразную защитную корочку, а кроме того, уплотняют слой покрытия, обеспечивая снижение его проницаемости. [21]
Продукты коррозии цинка хорошо растворимы и в кислотах, и в щелочах и экранируют поверхность металла лишь в нейтральных средах. [22]
Продукты коррозии цинка имеют щелочную реакцию, поэтому могут вызвать омыление некоторых лакокрасочных покрытий. При этом нарушается адгезия к металлу. Для снижения химической активности цинка и повышения защитных свойств поверхность оцинкованных деталей подвергают хроматной пассивации. Грунтовки и эмали на основе маслосодержащих пленкообразователей для защиты оцинкованных поверхностей не рекомендуются. [23]
Скорость коррозии цинка резко повышается при контакте его с более электроположительными металлами, поэтому в технике цинк применяют в качестве протектора для всех более благородных металлов, за исключением свинца. Следует отметить, что в зависимости от состава электролита, о чем указывалось выше, может произойти перераспределение потенциалов. В частности, в среде морской воды цинк является протектором для алюминия и его сплавов, хотя по ряду напряжений алюминий менее благороден, чем цинк. [24]
Скорость коррозии цинка в дистиллированной воде составляет 2 - 2 2 г / м2 - 24 ч; при длительной эксплуатации она уменьшается почти наполовину. При повышении температуры дистиллированной воды до 50 С скорость коррозии растет незначительно, а после 50 С быстро возрастает, достигая максимума примерно при 70 С, и в интервале температур 70 - 100 С уменьшается. [25]
Продукты коррозии цинка никогда не могут находиться на поверхности в совершенно сухом виде, так как 10 % - ной относительной влажности воздуха практически е бывает. Для кадмия, наоборот, требуется 90 % - ная влажность воздуха, чтобы гальванический элемент мог действовать. Это может быть не всегда даже в тропиках. Отсюда ясно, почему детали, имеющие кадмиевые покрытия, прекрасно зарекомендовали себя на океанских судах, в портах при обильном действии брызг морской воды и, наоборот, оказались неустойчивыми в условиях тропических лесов. [26]
На коррозию цинка большое влияние оказывает степень его чистоты и характер примесей. Примеси в цинке, для которых характерно высокое перенапряжение водорода, как, например, свинец, ртуть, уменьшают скорость растворения цинка в кислотах в том случае, если процесс коррозии протекает с водородной деполяризацией, но и в этих условиях цинк нельзя рассматривать как стойкий металл. Примеси железа, меди и других металлов, для которых характерно незначительное перенапряжение водорода, - вредны. [27]
Как происходит коррозия цинка, находящегося в контакте с кадмием в нейтральном и кислом растворах. [28]
Например, коррозия цинка в дистиллированной воде при температуре выше 50 С начинает сильно возрастать, достигает максимума и после 90 С резко падает почти до нуля. Это объясняется тем, что при температуре ниже 50 и выше 90 С продукты коррозии образуют пленку с высокими заш итными свойствами, а в интервале 50 - 90 С образуется пленка пористая с плохими защитными свойствами. [29]
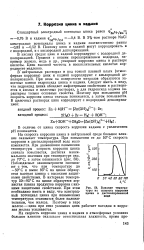 |
Влияние температуры на скорость коррозии цинка в дистиллированной воде. [30] |
Страницы: 1 2 3 4 5