Коррозия - цинк
Cтраница 3
На скорость коррозии цинка в нейтральной среде большое влияние оказывает температура. При повышении ее до 50 С скорость коррозии в дистиллированной воде мало изменяется. Наблюдаемые закономерности связывают с тем, что при температуре до - 50 С и выше 95 С на цинке образуется плотная пленка с высокими защитными свойствами. В интервале температур 50 - 95 С на цинке образуется зернистая пленка продуктов коррозии с низкими защитными свойствами. При этом необходимо иметь в виду, что электродный потенциал цинка при повышенных температурах становится более положительным, чем железа. [31]
Поэтому скорость коррозии цинка вновь возрастает при переходе от нейтральных к щелочным растворам. [32]
Во время коррозии цинка на его поверхности иногда образуются белые пятна ( белый порошок), так называемая белая ржавчина, для борьбы с которой стальные изделия, покрытые цинком, следует помещать в условия, обеспечивающие циркуляцию воздуха. [33]
Почему скорость коррозии цинка различна в контакте с разными металлами. [34]
Он вызывает коррозию цинка и не защищает алюминий. Пригоден для пассивирования в условиях межоперационного хранения. Триэтаноламин и моноэтаноламин защищают только черные металлы и вызывают коррозию цветных. Применяются в условиях межоперационного хранения, позволяют исключить операцию промывки и сушки. Танин применяется при длительном хранении изделий из черных металлов. [35]
Сероводород вызывает коррозию цинка, железа, меди, латуни, алюминия и других металлов с образованием сульфидов этих металлов. [36]
В присутствии SOb коррозия цинка резко возрастает. [38]
Установлено, что коррозия цинка в везерометре в течение 12 ч соответствует коррозии цинка в промышленной атмосфере в течение двух лет. [39]
Рис - 2.2. Коррозия цинка на воздухе возможным. [40]
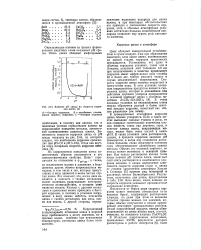 |
Влияние рН среды на скорость коррозии цинка. [41] |
В промышленных атмосферах коррозия цинка обычно ускоряется. В таких условиях цинк растворяется, однако, в процессе коррозии значение рН повышается, и когда оно становится достаточно большим, снова образуются основные соли, обеспечивающие дальнейшую защиту металла. Обычно это основной карбонат, но иногда может возникать и основной сульфат. [42]
 |
Схема перехода от разреза реальной корродирующей поверхности к модели.| Схема установки, применяющейся для измерения силы тока пары и потенциалов электрохимической пары. [43] |
Сравнивая рассчитанную скорость коррозии цинка с истинной, наблюдающейся на практике, например в озерной воде, соответствующей примерно составу нашего электролита, приходится заключить, что последняя во много раз меньше. [44]
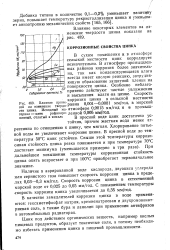 |
Влияние приме - rr n nrvl n пг м. [45] |
Страницы: 1 2 3 4 5
