Коррозия - цинк
Cтраница 4
В качестве замедлителей коррозии цинка в воде применяются: гексаметафосфат натрия, кремненатриевая и двухромовонат-риевая соль, а также бура и ланолин при применении антифризов в автомобильных радиаторах. [46]
На примере изучения коррозии цинка, алюминия и меди, проведенного в Кембридже в 1928 г. 2, можно показать, каким образом определяется характер и распределение разрушения для различных металлов в зависимости от свойств самого металла, его окислов и солей. Цинк и медь могут служить примером неблагородного и благородного конца ряда напряжений, а алюминий является металлом, хотя и находящимся в отрицательной части ряда, но обладающим значительной устойчивостью вследствие защитного характера своей пленки. Некоторые работы в других лабораториях с этими же металлами будут также упомянуты. [47]
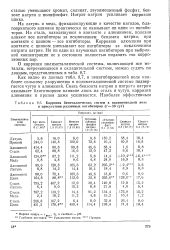 |
Коррозия биметаллических систем в водопроводной воде в присутствии различных ингибиторов ( 30 сут. [48] |
Нитрит атрия усиливает коррозию цинка. [49]
 |
Коррозия цинка, соприкасающегося с раствором сульфата. [50] |
В этом процессе коррозию цинка вызывает сульфат меди. Электроны, переходящие от цинка к ионам меди, нейтрализуют последние. Возникающие при этом атомы меди не точно замещают переходящие в раствор атомы цинка ( рис. 30), не встраиваются в кристаллическую решетку цинка, а образуют микроскопически маленькие кристаллики меди, которые в качестве чужеродного тела прилипают к поверхности цинка, создавая более или менее рыхлущ пленку. [51]
Морская вода вызывает более слабую коррозию цинка, чем водные растворы хлоридов и сульфатов щелочных металлов. [52]
Саморазряд цинкового электрода ( коррозия цинка) усиливается в случае загрязнения цинка примесями с более низким перенапряжением выделения на них водорода, например железом. Примеси же металлов, обла - дающих большим перенапряжением выделения водорода, чем цинк, например ртути, уменьшают скорость растворения цинка. Последним обстоятельством пользуются в производстве элементов, амальгамируя цинковые электроды. [53]
Саморазряд цинкового электрода ( коррозия цинка) усиливается в случае загрязнения цинка примесями с более низким перенапряжением выделения на них водорода, например железом. Примеси же металлов, обладающих большим перенапряжением выделения водорода, чем цинк, например ртути, уменьшают скорость растворения цинка. Последним обстоятельством пользуются в производстве элементов, амальгамируя цинковые электроды. [54]
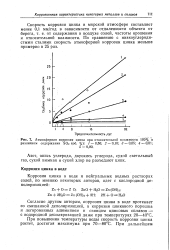 |
Атмосферная коррозия цинка при относительной влажности 100 % и различном содержании SO2 ( об. %. / - 0 50. 2 - 0 10. 3 - 0 05. nni. [55] |
Согласно другим авторам, коррозия цинка в воде протекает со смешанной деполяризацией, а коррозия цинкового порошка и легированных алюминием и свинцом цинковых сплавов - с водородной деполяризацией даже при температурах 20 - 40 С. [56]
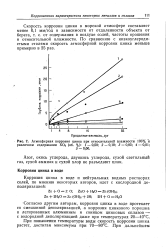 |
Атмосферная коррозия цинка при относительной влажности 100 % и различном содержании S02 ( об. %. 1 - 0 50. 2 - 0 10. 3 - 0 05. 4 - 0 01. [57] |
Согласно другим авторам, коррозия цинка в воде протекает со смешанной деполяризацией, а коррозия цинкового порошка и легированных алюминием и свинцом цинковых сплавов - с водородной деполяризацией даже при температурах 20 - 40 С. [58]
В природных водах скорость коррозии цинка в несколько раз меньше, чем скорость коррозии железа, причем наибольшая коррозионная стойкость цинка проявляется при рН 9 - Ml. В интервале от 50 до 90 С слой продуктов коррозии цинка имеет зернистую структуру и плохо сцеплен с поверхностью металла, что и ведет к усиленной коррозии последнего. При темпе - - ратурах ниже 50 и выше 90 С образуется хорошо сцепленная с поверхностью плотная пленка продуктов коррозии. Это явление может привести к-нарушению работы оборудования теплоцентралей, где используются оцинкованные стальные трубы и конструкции. [59]
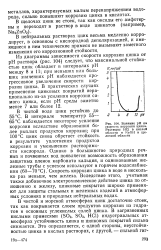 |
Влияние рН на скорость коррозии цинка. Растворы НС1 в кислой области и NaOH в щелочной области. [60] |
Страницы: 1 2 3 4 5