Коэффициент - поверхностная диффузия
Cтраница 3
Изучение энтропии адсорбции дает полезную, но только качественную информацию о подвижности адсорбированных мономеров. Наиболее прямую информацию дает непосредственное изучение коэффициентов поверхностной диффузии. [31]
Высокая концентрация вакансий и увеличение расстояния между узлами способствуют увеличению коэффициента объемной диффузии и по вакансиям и по междоузлиям, а также коэффициента обменной диффузии. На рис. 50 показана температурная зависимость коэффициентов объемной и поверхностной диффузии и диффузии по границам зерен. [32]
 |
Коэффициенты диффузии н. бутана в силикагеле. [33] |
Энергия активации, найденная из температурной зависимости коэффициента поверхностной диффузии, составила Е - 3950 кал / моль. Для образца с пористостью 8 0 53 и температур ниже - 30 С получено более низкое значение Е - 2900 кал / моль. [34]
Состояние окружающей среды и, в частности, степень разрежения оказывает влияние на механические свойства металлов и сплавов, что обусловлено изменением поверхностной энергии на межфазной границе. Одним из критериев оценки энергетического состояния поверхности является коэффициент поверхностной диффузии. [35]
Через us обозначена поверхностная скорость, a Ds - коэффициент поверхностной диффузии поверхностно-активного вещества. Обычно полагают, что / ditf - 0, поскольку конвективный поток является превалирующим. Это упрощение может быть сделано лишь в случае, если поверхностно-активное вещество является растворимым. Поток массы из объема определяется скоростями диффузии и адсорбции. [36]
При рассмотрении моделей адсорбции и анализе энтропии адсорбции нередко говорят о подвижной и локализованной адсорбции ( см. гл. По аналогии с текучестью объемной фазы более прямым критерием подвижности адсорбата является коэффициент поверхностной диффузии. [37]
С другой стороны, у металлов III группы при температурах конденсации ниже комнатной, по-видимому, может образоваться нетекстури рованный конденсат. Указанные наблюдения могут быть объяснены увеличением энергии связи и, следовательно, уменьшением коэффициента поверхностной диффузии. [38]
Можно думать, что в недалеком будущем этим методом удастся получить не только качественные, но и количественные данные, например, определить коэффициенты поверхностной диффузии наподобие того, как это было осуществлено в классических работах Фольмера при помощи светового микроскопа. Отсутствие до сих пор таких работ связано с методическими трудностями - необходимостью помещать объект в вакуум и с действием электронного облучения на него, приводящего, в частности, к покрытию объекта углеродной пленкой. Это затрудняет последовательнее изучение одних и тех же мест препарата после каких-либо обработок его вне микроскопа с целью фиксирования изменений структуры. В работах [57, 58] это затруднение было обойдено путем термической обработки препаратов, причем загрязняющий слой углерода выгорал. Успехи в конструировании газовой камеры и приспособлений для нагревания объекта в микроскопе позволяют надеяться, что в дальнейшем удастся осуществить прецизионные количественные измерения поверхностной диффузии в самом электронном микроскопе. [39]
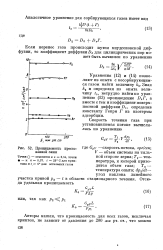
Уравнения ( 12) и ( 14) позволяют из опыта с несорбирующимся газом найти величину &2. Зная / е2 и определяя из опыта величину t3, нетрудно найти по уравнению ( 13) произведение DSP, a вместе с тем и коэффициент поверхностной диффузии Ds, определив константу Генри Г из изотермы адсорбции. [41]
В рамках предложенной теории роста графита эффект фракционирования находит свое объяснение. Действительно, графит обогащается легким изотопом углерода ( в противоположность алмазу) по сравнению с исходным метаном лишь при малых скоростях роста, когда процесс лимитируется двумерным зародышеобразованием из адсорбированного газа. Тогда скорость роста зародышей пропорциональна коэффициенту поверхностной диффузии, который, в свою очередь, пропорционален корню квадратному из массы молекулы. При больших скоростях роста, когда скорость реакции зависит от потока атомов углерода на поверхность, растущий графит наследует изотопный состав углеродного газа. [42]
 |
Влияние легирующих ( третьих [ IMAGE ] Схема диффузии по поверх. [43] |
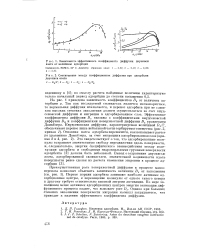
Поверхностную диффузию, кроме того, ускоряет большая подвижность поверхностных слоев атомов. В качестве примера на рис. 97 показаны кривые температурной зависимости коэффициентов диффузии тория в вольфрам: / - поверхностной, 2 - по границам зерен и 3 - объемной. Максимальные значения во всех областях температур имеют коэффициенты поверхностной диффузии, несколько меньшие - коэффициенты диффузии по границам зерен; наиболее медленно протекают объемные диффузионные процессы. [44]
 |
Зависимость эффективного коэффициента диффузии двуокиси азота от величины адсорбции. [45] |
Страницы: 1 2 3 4