Коэффициент - распределение - металл
Cтраница 1
Коэффициенты распределения металлов при экстракции из растворов азотной кислоты, как травило, значительно ниже. При частичной замене кислоты солью извлечение может увеличиваться. Эффект зависит от природы катиона-шысал-июателя, и зависимость эта трудно объяснима. Из растворов серко - и хлорокислых растворов металлы экстрагируются хуже, чем из азотнокислых. [1]
Коэффициенты распределения металла зависят от температуры, времени контакта фаз, если равновесие устанавливается не мгновенно, от состава водной фазы, если она содержит не только галогеноводород-ную кислоту. [2]
Линейная зависимость коэффициента распределения металла от СА нарушается тогда, когда в качестве растворителя используется спирт, приводящий к мономеризации алкилфосфорной кислоты [4, 13, 15], и когда См становится соизмеримой с СА [5], что полностью согласуется с предложенным нами способом трактовки данных по экстракции ассоциированными расчетами. [3]
Линейная зависимость коэффициента распределения металла от Сд нарушается тогда, когда в качестве растворителя используется спирт, приводящий к мономеризации алкилфосфорной кислоты [4, 13, 15], и когда См становится соизмеримой с Сд [5], что полностью согласуется с предложенным нами способом трактовки данных по экстракции ассоциированными расчетами. [4]
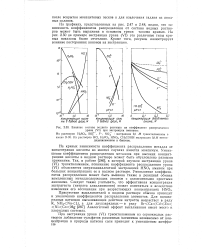 |
Влияние состава водного раствора на коэффициент распределения. [5] |
На кривых зависимости коэффициента распределения металла от концентрации кислоты во многих случаях имеется максимум. Уменьшение коэффициентов распределения металлов при высоких концентрациях кислоты в водном растворе может быть обусловлено разными причинами. Так, в работе [286], в которой изучали экстракцию урана ( VI) триоктиламином, понижение коэффициента распределения урана ( VI) объясняется сверхэквивалентной экстракцией HNOs амином при больших концентрациях ее в водном растворе. Уменьшение коэффициентов распределения может быть вызвано также и реакцией обмена комплексных металлсодержащих анионов с одноименными простыми анионами. [6]
По данным зависимости коэффициента распределения металла от равновесной концентрации лиганда с помощью расчетных методов Ледена, Бьеррума и Дюрссена - Силлена были рассчитаны значения констант устойчивости. [7]
В таблице 1 приведены коэффициенты распределения металлов между некоторыми ионитами и цитратными растворами. В сорбируемо-сти металлов катионитами из неразбавленного и разбавленного водой ( 1: 1) реактива Петермана найдены различия, перспективные для хро-матографического разделения. Например, катионит КУ-1 поглощает из реактива Петермана Си, тогда как Mn, Co, iNi не поглощаются катиони-том, a Fe, Al, Са сорбируются незначительно. Из разбавленного водой ( 1: l) реактива Петермана Си и Zn сорбируются катионитами лучше других металлов. [8]
При повышении концентрации кислот коэффициенты распределения металлов, как правило, уменьшаются, что может быть обусловлено конкурирующей экстракцией кислот. Если кислоту частично заменить на какую-либо соль этой кислоты, то снижение коэффициента распределения металла при увеличении концентрации кислоты проявляется меньше. [9]
При выводе формул, связывающих коэффициент распределения металла ( D) с концентрацией лигандов, необходимо учитывать ряд равновесных реакций. [10]
Имеющийся экспериментальный материал о зависимости коэффициентов распределения металлов от их концентрации хорошо согласуется с приведенной выше схемой. При экстракции комплексных металлгалогенидных кислот низкополярными простыми эфирами коэффициенты распределения постоянны при низких концентрациях металла, но затем растут с увеличением концентрации металла. [11]
В этом методе изучается зависимость коэффициента распределения металла ксмплексообразователя между катионитом и раствором, затем в растворе того же состава между анионитом и раствором от концентрации адденда в исходном растворе при постоянной ионной силе раствора. [12]
Все упомянутые уравнения выведены при условии постоянства коэффициента распределения металла, что вполне оправдано при экстракции элементов, находящихся в растворе в микроколичествах. Однако в общем случае это условие не соблюдается. Переменный коэффициент распределения, по-видимому, также может быть одной из причин нелинейности зависимости в полулогарифмических координатах. Последняя может наблюдаться также и при диффузионном режиме, когда коэффициенты массопередачи изменяются с изменением движущей силы, например при наличии спонтанной конвекции. [13]
В общем, несмотря на большое разбавление ТОФО, порядок величины для коэффициентов распределения металлов приблизительно совпадает со значениями, приведенными на рис. 5 и 6, для систем с неразбавленным ТБФ. [14]
Таким образом, при экстракции, основанной на потере сродства к воде, коэффициент распределения металла зависит от концентрации реагента в органической фазе и от кислотности водного раствора. [15]
Страницы: 1 2 3 4