Коэффициент - распределение - металл
Cтраница 3
Коэффициенты распределения металлов между катионитом и хлор-нокислым раствором в присутствии комплексонов значительно меньше, чем в их отсутствие, что свидетельствует о комплексообразо-вании гафния и циркония с комплексонами. Предполагалось, что катионитом сорбируются только ионы металла, комплексные ионы не сорбируются. [31]
Очень трудно сделать какие-либо выводы о степени сольватации гидратпрованных галоид-металлических кислот в органическом рас - творе. Однако коэффициент распределения металла иногда [208, 220] является линейной функцией концентрации кислородсодержащего экстрагента, если в качестве разбавителя используются углеводороды. [32]
На кривых зависимости коэффициента распределения металла от концентрации кислоты во многих случаях имеется максимум. Уменьшение коэффициентов распределения металлов при высоких концентрациях кислоты в водном растворе может быть обусловлено разными причинами. Так, в работе [286], в которой изучали экстракцию урана ( VI) триоктиламином, понижение коэффициента распределения урана ( VI) объясняется сверхэквивалентной экстракцией HNOs амином при больших концентрациях ее в водном растворе. Уменьшение коэффициентов распределения может быть вызвано также и реакцией обмена комплексных металлсодержащих анионов с одноименными простыми анионами. [33]
Миллс и Логан изучили некоторые закономерности образования третьей фазы при экстракции нитратов тория, уранила, плутония и плутонила из азотнокислых растворов 20 % - ными ( по объему) растворами ТБФ в керосине. В опытах определялся коэффициент распределения металлов при увеличении их концентрации с 10 г / л до величины, при которой наблюдается образование третьей фазы. [34]
Этот вопрос еще не вполне строго можно объяснить теоретически. Установлено, что коэффициент распределения металла между ионитом и раствором определяется коэффициентом избирательности, долей поглощаемой формы металла и отношением концентрации лиганда ( адденда) в ионите и растворе. [35]
Конечно, уравнение ( 1) справедливо независимо от того, присутствуют ли другие соединения металла и реагента в системе. При некоторых условиях оно непосредственно выражает коэффициент распределения металла, который для аналитика представляет основной интерес. Коэффициент распределения в9 Е представляет отношение равновесных концентраций одного и того же вещества, присутствующего в любых формах в обеих фазах несмешивающихся растворителей. [36]
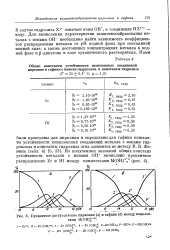 |
Процентное распределение циркония ( а и гафния ( б между комплек. [37] |
В случае гидролиза X г - означает ионы ОН, а соединение НХ1 z - воду. Для вычисления характеристик комплексообразования металла с ионами ОН необходимо найти зависимость коэффициентов распределения металла от рН водной фазы при постоянной ионной силе, а также постоянных концентрациях металла в водной фазе и ( 3-дикетона в слое органического растворителя. [38]
При повышении концентрации кислот коэффициенты распределения металлов, как правило, уменьшаются, что может быть обусловлено конкурирующей экстракцией кислот. Если кислоту частично заменить на какую-либо соль этой кислоты, то снижение коэффициента распределения металла при увеличении концентрации кислоты проявляется меньше. [39]
Эти данные могут быть получены криоскопическим, эбулиоскопическим или другим методом. Для расчета второго члена правой части уравнения (11.91) в частном случае, когда коэффициент распределения металла не зависит от его концентрации, значение din ас / дтс можно взять из описания двухкомпонентной системы, используя и в этом случае уравнение Гиббса - Дюгема. [40]
При добавлении А ( вспомогательное комплексообразующее вещество, являющееся маскирующим веществом) должен увеличиваться только коэффициент распределения РА маскируемого металла, но не коэффициент распределения РА определяемого металла, и отношение констант должно возрасти по крайней мере до величины 104 - 105 для того, чтобы ошибка титрования, согласно уравнению ( 72), была небольшой. При этом следует различать полное и частичное маскирование мешающего металла. При первом / См г становится настолько малой, что М вообще не реагирует с титран ом, тогда как при частичном маскировании после полного завершения образования комплекса металла М с титрантом последний реагирует также с М и может оказаться возможным последовательное титрование. [41]
Из уравнения (2.83) следует, что для определения состава и констант устойчивости возникающих комплексов достаточно измерить коэффициенты распределения металла при разных рН и концентрации. [42]
Если концентрация реагента постоянна, а концентрация металла изменяется ( превышает концентрацию реагента или становится немного меньше ее), то коэффициент распределения металла оказывается зависящим от общей концентрации его в двухфазной системе. [43]
Многие внутрикомплексные соединения, в которых ион металла окружен анионными лигандами, число которых достаточно для нейтрализации его положительного заряда и заполнения всех координационных мест, легко экстрагируются из водных растворов органическими растворителями. При объединении уравнений ( 1) и ( 2) становится видно, что если в комплекс входят п однозарядных ионов лигандов, то коэффициент распределения металла в присутствии избытка реагента будет функцией га-й степени от концентрации иона водорода. [44]
Механизм экстракции металлов при помощи ТОФО соответствует общей схеме, предложенной для нейтральных фоофороргани-ческих экстрагентов ( см. разд. Если продолжить сравнение с ТБФ, то следует подчеркнуть, что значительное различие между ними проявляется при экстракции минеральных кислот, в то время как коэффициенты распределения металлов заметно выше. [45]
Страницы: 1 2 3 4