Коэффициент - распределение - элемент
Cтраница 2
 |
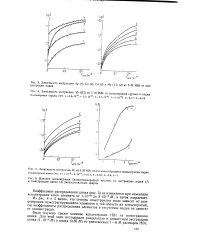
Экстракция кобальта из роданидных растворов различными растворителями. Концентрация кобальта 1 мг / мл, рН 2 7. [16] |
Было показано [579], что в системе амиловый спирт - раствор NH4SCN зависимость коэффициентов распределения элементов от концентрации SCN-ионов аналогична такой же зависимости для Rf элементов на бумажных хроматограммах. [17]
Таким образом, изменение органического радикала в молекуле экстрагента в различной степени влияет на коэффициенты распределения элементов, причем изменение длины алкильного радикала оказывает на фактор разделения более сильное влияние, чем электроотрицательность арильнога радикала. [18]
Таким образом, изменение органического радикала в молекуле экстрагента в различной степени влияет на коэффициенты распределения элементов, причем изменение длины алкильного радикала оказывает на фактор разделения более сильное влияние, чем электроотрицательность арильного радикала. [19]
Для примесей, сокристаллизующихся с алюминием ( группа III Б), в значениях коэффициентов распределения элементов малых периодов наблюдается по одному максимуму: из элементов второго периода наибольшее значение приходится на коэффициент распределения бериллия, а из третьего периода-на коэффициент распределения магния. Для примесей-элементов больших периодов наблюдаются по два максимума. Вторые максимумы приходятся на примеси меди, цинка, германия в четвертом периоде, на примеси серебра, кадмия и индия ( пятый период), на примеси свинца и висмута ( шестой период), однако численные значения коэффициентов распределения этих элементов меньше, чем для элементов, на которые приходятся первые максимумы. [20]
В литературе по ионному обмену и по ионообменной хроматографии приводится довольно много данных по коэффициентам распределения элементов между смоляной фазой и раствором в различных условиях проведения опыта; такой подход отвечает аналогии ионообменных процессов с экстракцией, до сих пор, к сожалению, не рассмотренной с достаточной полнотой с научной точки зрения. [21]
 |
Сорбция фенантролината Fez катионитом КУ-2 из растворов А1С1з в различных средах. [22] |
Однако в связи с большими различиями в ионных радиусах коэффициенты распределения примесей оказались значительно выше коэффициентов распределения элементов матрицы, благодаря чему оказалось возможным их количественное выделение. На рис. 2.3 показана сорбция Fe2 из соединений алюминия. Видно, что в широком интервале рН в течение 2 ч достигалась полнота сорбции; аналогичная картина наблюдается для остальных примесей и в случае других элементов матрицы. Более того, фенантролинаты примесей оказались очень прочно связанными с катионитом, благодаря чему его можно было отмывать от элементов матрицы, не теряя при этом примесей. Даже при промывке катиони-та достаточно концентрированными кислотами потери не превышают нескольких процентов, что при спектральном анализе концентрата не имеет существенного значения. [23]
В некоторых случаях при экстракции из азотной ( или соляной) кислоты высокой концентрации наблюдается увеличение коэффициентов распределения элементов, что объясняется образованием комплексов типа M ( NO3) A ( H. Подтверждением такого механизма служит обнаружение анионов соответствующих кислот в органической фазе. [24]
Другими исследователями [33, 34] также отмечается, что в колонках, наполненных сополимерами стирола с ДВБ, обработанными экстрагентом, коэффициенты распределения элемента заметно ниже, чем для такого же экстрагента в статической экстракции. Поэтому расчет условий хроматографического разделения из данных по статической экстракции затрудняется. Однако более прочная связь экстрагента с носителем приводит к меньшей растворимости экстрагента в элюентах, чем при хроматографии на колонках, заполненных другими носителями, или чем растворимость экстрагента в условиях статической экстракции. [25]
Из применяемых в хроматографии методов определения сорбцяонной способности элемента мы считаем наиболее простым и удобным для практических целей метод определения коэффициентов распределения элемента между ионитом и раствором. [26]
Приводятся данные об анионах, в виде которых металл находится в составе экстрагирующихся соединений, и данные о типе зависимости коэффициента распределения элемента от концентрации кислоты, включающей анион-лиганд, в водной фазе. Зависимости типов А, Б, В различаются положением максимума коэффициента распределения. Для зависимостей типа А максимум коэффициента распределения соответствует самым низким концентрациям аниона-лиганда, и практически при увеличении концентрации кислоты наблюдается только снижение коэффициента распределения. Для зависимостей типа Б максимум находится при средних концентрациях анионов-лигандов. [27]
Из рис. 4 и 5 видно, что степень соэкстракции мало зависит от концентрации соэкстрагирующихся элементов в той области их концентраций, где коэффициенты распределения элементов в отсутствие индия не зависят от концентрации. [29]
Значения Rf в ламинарной хроматографии количественно связаны с удерживаемыми объемами VR для данного элемента в аналогичных колоночных системах, поскольку как Rf, так и VR в свою очередь определяются коэффициентами распределения элемента D между органической и водной фазами. [30]
Страницы: 1 2 3 4