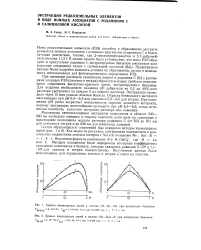
Молярный коэффициент - погашение - комплекс
Cтраница 2
В методе, предложенном Пиленом и Конником1 для вычисления молярного коэффициента погашения комплекса циркония с теноилтрифторацетоном ( ТТА), используется константа распределения этого комплекса между двумя растворителями. [16]
В методе, предложенном Циленом и Конником [10], для вычисления молярного коэффициента погашения комплекса циркония с тено-илтрифторацетоном ( ТТА) используют константу распределения этого комплекса между двумя растворителями. [17]
 |
Определение алюминия в стали со стильбазо. [18] |
Чувствительность реакции, по нашим наблюдениям, составляет 0 04 - [ 1мл А1; молярный коэффициент погашения комплекса равен 1 5 104; максимальная интенсивность окраски наблюдается при рН 5 2 - 5 6 через 10 мин. Интервал подчиняемости закону Бзра отвечает 0 1 - 1 - ( / мл А1; при больших концентрациях алюминия пропорциональности между концентрацией и величиной оптической плотности не наблюдается. Железо реагирует со стильбазо в том же интервале рН, что и алюминий с образованием грязно-коричневой окраски. Количественное определение алюминия со стильбазо рекомендуется производить методом шкалы или фотометрического титрования [16]; предложены фотометрические методы [14-16] определения алюминия в стали при помощи стильбазо. [19]
Оптимальное значение рН для определения скандия этим методом составляет 1 5 - 3 0; молярный коэффициент погашения комплекса е 2 9 - Ю4 при Х акс 640 нм. [20]
При определении бериллия с помощью бериллона II [24, 25] цветную реакцию проводят при рН 12 - 13; молярный коэффициент погашения комплекса составляет 1 2 - 10 при Х макс 630 нм. [21]
Здесь п - количество связанных с центральным атомом молекул реагента; ЕНА - молярный коэффициент погашения реагента на максимуме поглощения; еМА - молярный коэффициент погашения комплекса на максимуме полосы, которая по своему происхождению соответствует упомянутой выше полосе поглощения реагента. [22]
ЭДТА ( - 0 006 М) при рН 4 ч - 6 и цианид-ионы при рН - 7 - ь 11 не влияют на экстракцию Cd. Молярный коэффициент погашения комплекса при К 262 нм равен 32 70Q Комплекс очень устойчив. [23]
Среди прочих оксисоединений, применяемых в качестве аналитических реагентов на титан, особого внимания заслуживает хромотроповая кислота. Молярный коэффициент погашения комплекса, образуемого титаном с хромотроповой кислотой, согласно данным А. К. Бабко и П. В. Ходулиной [4], примерно в 100 раз выше, чем перекисного комплекса титана. [24]
Определение бария и стронция с реагентом диметилсульфоназо III основано на образовании окрашенных комплексов бария в водной среде и стронция в водно-ацетоновой среде. Молярные коэффициенты погашения комплексов в нейтральном водном растворе равны соответственно: с барием - 13 9 - 103, со стронцием - 6 - Ю3; в 35 - 40 % - ном ацетоне - 28 8 - 103 и 34 4 - 103 соответственно. [25]
Цветная реакция арсеназо III с РЗЭ представляет интерес в том отношении, что в области максимума поглощения комплекса ( h 650 нм) сам реагент практически не поглощает. Молярные коэффициенты погашения комплексов других РЗЭ имеют близкие значения. [26]
В уксуснокислой среде ( рН 5 - 6) сульфоназо не реагируете иттрием, и поэтому его можно применять для определения скандия после выделения в виде тарт-рата с иттрием в качестве носителя. Молярный коэффициент погашения комплекса сульфоназо со скандием составляет 1 0 - 10 при Ямакс 575 нм. [27]
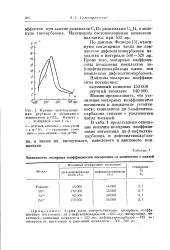 |
Зависимость молярных коэффициентов погашения от количества л-связей. [28] |
По данным Фишера [5], максимумы поглощения таких же комплексов дифенилтиокарбазона находятся в интервале 500 - 520 мц. Кроме того, молярные коэффициенты погашения комплексов ди - - нафтилтиокарбазона выше, чем комплексов дифенилтиокарбазона. [29]
Страницы: 1 2 3 4