Средний ионный коэффициент - активность
Cтраница 2
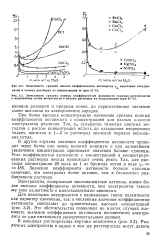
При более высоких концентрациях изменение средних ионных коэффициентов активности с концентрацией для разных классов электролитов различно. Так, у сульфатов тяжелых цветных металлов с ростом концентрации вплоть до насыщения непрерывно падает, достигая в 1 - 2 т растворах значений порядка нескольких сотых. [17]
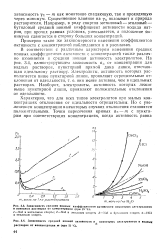
В соответствии с различным характером изменения средних ионных коэффициентов активности с концентрацией также различно изменяется и средняя ионная активность электролитов. На рис. 3.4, иллюстрирующем зависимость а от концентрации для водных растворов, пунктирной прямой дана линия, отвечающая идеальному раствору. Наоборот, электролиты, активность которых лежит выше пунктирной линии, проявляют положительные отклонения от идеальности. [19]
Таким образом, в принципе можно определить средний ионный коэффициент активности электролита, поделив реалыто наблюдаемое данление пара электролита над растнором на давление пара над идеальным рас-тно-ром, которое можно найти, определив km экстраполяцией па очень разбавленные растворы ( ср. Практически более точными и легче осуществимыми являются методы, описываемые в следующих двух параграфах. [20]
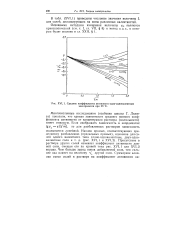 |
Средние коэффициенты активности одно-одновалентных электролитов при 25 С. [21] |
Льюиса) показали, что кривая зависимости среднего ионного коэффициента активности от концентрации раствора ( моляльности) имеет минимум. [22]
В табл. 10 приведены результаты потенциометриче-ского определения среднего ионного коэффициента активности серной кислоты в моляльной шкале концентраций в несимметричной системе стандартных состояний. [23]
Полагаем, что коэффициенты активности ионов равны средним ионным коэффициентам активности. [24]
Выше приняты следующие обозначения: уг - - средний ионный коэффициент активности компонента г; F. [25]
Очевидно, что аналогичное равенство справедливо и для средних ионных коэффициентов активности. Отсюда следует, что при обычном выборе стандартного состояния электролита можно, исходя из справочных сведений о средних коэффициентах активности Y, вычислить значение реального коэффициента активности у одного из составляющих электролит ионов, если известен реальный коэффициент активности у 2 противоиона. [26]
Во всех очень разбавленных растворах электролитов при равной ионной силе средние ионные коэффициенты активности электролитов одного и того же типа валентности численно одинаковы. [27]
Этот принцип можно сформулировать следующим образом: в области разбавленных растворов средний ионный коэффициент активности сильного электролита имеет одинаковую величину во всех растворах одинаковой ионной силы. Следовательно, важнейшей характеристикой, определяющей активность электролита в растворе, является не концентрация его, а ионная сила. [28]
В литературе можно часто встретить эту формулу со знаком минус перед логарифмом среднего ионного коэффициента активности. [29]
Оценку коэффициента активности хлорид-иона обычно делают по уравнению Дебая - Хюккеля или приравнивают среднему ионному коэффициенту активности НС1 в водном растворе кислоты с такой же ионной силой, какую имеет буферный раствор. [30]
Страницы: 1 2 3 4