Средний коэффициент - активность - электролит
Cтраница 2
В частности, они нашли, что в области низких концентраций средние коэффициенты активности электролита определяются валентностью образующихся ионов и не зависят от других их свойств. Так, например, в этих условиях средние коэффициенты активности бромида калия, нитрата натрия и соляной кислоты одинаковы. Зависимость среднего коэффи - не от химической природы циента активности 1 - 1 валентного ЧГТРК-ТППГТИТЛК R гяячи г атим электролита от концентрации электролитов. [16]
Для разбавленных растворов электролитов экспериментальным путем установлен закон ионной силы; средний коэффициент активности электролита определяется только ионной силой раствора и не зависит от природы и концентрации отдельных ионов. [17]
Поскольку коэффициенты активности отдельных ионов термодинамически неопределимы, часто вместо них используют средние коэффициенты активности электролита в целом. [18]
Поскольку коэффициенты активности отдельных ионов термодинамически неопределимы, то часто вместо них используют средние коэффициенты активности электролита в целом. [19]
На основании этого уравнения из стандартного коэффициента активности при данных условиях можно вычислить относительный средний коэффициент активности электролита, полагая, что 1 моль электролита гидра-тйрован h молями воды. [20]
Подставим в полученное уравнение а miYi, где т - средняя мо-ляльность; yi - средний коэффициент активности электролита. [21]
Метод вычисления коэффициента активности по экспериментальным данным [ см. уравнение (8.7) ] позволяет определить лишь значения средних коэффициентов активности электролита. В настоящее время не существует методов экспериментального определения коэффициентов активности отдельных ионов. При необходимости расчета этих величин обычно принимают, что средний коэффициент активности электролита представляет собой среднее геометрическое коэффициентов активности образующих его ионов. [22]
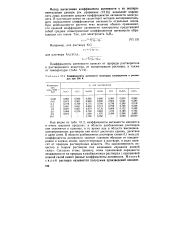 |
Коэффициенты активности некоторых электролитов в растворах при 298 К. [23] |
Метод вычисления коэффициента активности Y по экспериментальным данным [ см. уравнение (VI.8) ] позволяет определить лишь значения средних коэффициентов активности электролита. В настоящее время не существует методов экспериментального определения коэффициентов активности отдельных ионов. При необходимости расчета этих величин обычно принимают, что средний коэффициент активности электролита представляет собой среднее геометрическое коэффициентов активности образующих его ионов. [24]
Электростатическая теория разбавленных растворов сильных электролитов, развитая Дебаем и Гюккелем в 1923 г., позволила теоретически вычислить средний коэффициент активности электролита, эквивалентную электропроводность сильных электролитов, а также теоретически обосновала правило ионной силы. [25]
Из этого соотношения видно, что различие между ГА и ГА ( В) тем больше, чем сильнее зависит от концентрации органического вещества средний коэффициент активности электролита - у и чем выше концентрация ( точнее активность) этого вещества. Как показывает анализ, для органических веществ с высокой поверхностной активностью и, следовательно, достаточно малой концентрацией в растворе различиями в величинах ГА и ГА ( В можно пренебречь. [26]
Авторы [94] резонно замечают, что хотя представление о росте эффективной концентрация ионов по отношению к свободной воде, на котором базируется теория Стокса - Робинсона, и позволяет объяснить увеличение среднего коэффициента активности электролита с ростом его концентрации, однако на этой основе нельзя понять природу существенных различий в значениях Y и Y - поскольку связывание воды в гидратных оболочках ионов одинаково сказывается на эффективной концентрации катионов и анионов. [27]
Для многокомпонентных растворов электролитов с любым числом ионов, в том числе и для электролитов, не имеющих общих ионов, Мейсснером, Казиком и Тестером [17, 18] предложен приближенный способ вычисления приведенного среднего коэффициента активности электролита, обозначаемого Г с нижними нечетными индексами для катионов и четными для анионов. Первыми пишутся индексы для катионов. [28]
В табл. 10 приведены средние коэффициенты активности для ряда электролитов. Во всех случаях средний коэффициент активности электролита равен среднему геометрическому из коэффициентов активности ионов, на которые этот электролит диссоциирует в растворе. [29]
Ввиду широкого применения ионных ПАВ ( часто в смесях с другими электролитами) необходимо обсудить приложение уравнения (5.1) к электролитам. На практике пользуются средними коэффициентами активности электролита, а потому и уравнение адсорбции Гиббса желательно привести к соответствующей форме. [30]
Страницы: 1 2 3 4