Средний коэффициент - активность - электролит
Cтраница 3
Уравнение ( VII, 50) применимо только к сильно разбавленным электролитам и называется предельным законом Дебая - Гюккеля. При данной ионной силе раствора средний коэффициент активности электролита в предельно разбавленном растворе является величиной постоянной и не зависит от природы других электролитов в растворе. Таким образом, в предельном законе Дебая - Гюккеля получает теоретическое обоснование правило ионной силы. [31]
Чтобы по возможности строго судить, соответствуют ли изменения потенциала стеклянного электрода функции натриевых электродов, были приняты во внимание изменения коэффициентов активности ионов натрия в растворах. Значения последних принимались численно равными средним коэффициентам активности электролитов, в которые входят ионы натрия. Расчеты показали, что зависимость потенциала стеклянного электрода от логарифма активности ионов натрия в растворе приближается к линейной. Однако рассмотренная выше нормировка коэффициентов активности ионов была принята произвольно, а поэтому доказательство натриевой функции стеклянных электродов, данное в этой работе, не может считаться термодинамически строгим. [32]
Чтобы по возможности строго судить, соответствуют ли изменения потенциала стеклянного электрода функции натриевых электродов, были приняты во внимание изменения коэффициентов активности ионов натрия - в растворах. Значения последних принимались численно равными средним коэффициентам активности электролитов, в которые входят ионы натрия. Расчеты показали, что зависимость потенциала стеклянного электрода от логарифма активности ионов натрия в растворе приближается к линейной. Однако рассмотренная выше нормировка коэффициентов активности ионов была принята произвольно, а поэтому доказательство натриевой функции стеклянных электродов, данное в этой работе, не может считаться термодинамически строгим. [33]
Прежде чем рассматривать сам метод Бейтса - Робинсона, следует кратко охарактеризовать теорию гидратации ионов Стокса - Робинсона [ 22, гл. Указанная теория, предложенная для вычисления средних коэффициентов активности электролитов и описания их концентрационной зависимости, исходит из предположения о достаточно строгой применимости теории сильных электролитов Дебая - Хюккеля не только к разбавленным, но и к умеренно концентрированным растворам при следующих условиях: 1) учитывается связывание части молекул воды в гидратных оболочках ионов, которое приводит к уменьшению содержания в растворе свободной воды и к соответствующему изменению концентрации электролита; 2) теория Дебая - Хюккеля применяется не к свободным, а к гидратированным ионам электролита. [34]
В - теоретический коэффициент, равный для водных растворов при 25 0 33 - 108; а - средний эффективный диаметр ионов; он находится из опыта. Уравнение ( VII, 52) удовлетворительно согласуется со средними коэффициентами активности электролита, когда коэффициент активности уменьшается с увеличением концентрации электролита. [35]
В частности, было найдено что в области низких концентраций средние коэффициенты активности электролита определяются зарядами образующихся ионов и не зависят от других их свойств. Так, например, в этих условиях средние коэффициенты активности бромида калия, нитрата натрия и соляной кислоты одинаковы. Далее было-установлено, что средние коэффициен-ы активности для очень разбавленных растворов зависят от общей концентрации всех присутствующих электролитов и зарядов их ионов, но не от химической природы электролитов. [36]
В частности, было найдено что в области низких концентраций средние коэффициенты активности электролита определяются зарядами образующихся ионов и не зависят от других их свойств. Так, например, в этих условиях средние коэффициенты активности бромида калия, нитрата натрия и соляной кислоты одинаковы. Далее было установлено, что средние коэффициенты активности для очень разбавленных растворов зависят от общей концентрации всех присутствующих электролитов и зарядов их ионов, но не от химической природы электролитов. [37]
Вывод формулы для парциального давления электролита ( вследствие появляющейся при этом проблемы нормировки) является несколько громоздким, и он здесь приведен не будет. Заметим лишь, что соотношение между парциальным давлением р2 и средним коэффициентом активности электролита в растворе содержит множитель, зависящий от температуры, который ( как и в предыдущем примере) можно определить экстраполяцией измерений на бесконечное разбавление. [38]
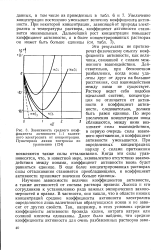 |
Зависимость среднего коэффициента активности 1 - 1 валентного электролита от концентрации. Пунктирная линия построена по уравнению ( 124. [39] |
В частности, они нашли, что в области низких концентраций средние коэффициенты активности электролита определяются лишь валентностью образующихся ионов и не зависят от других свойств. Так, например, в этих условиях средние коэффициенты активности бромида калия, нитрата натрия или соляной кислоты одинаковы. [40]
Поэтому средние коэффициенты активности определены термодинамически однозначно. Уравнение (50.11) приводит к примечательному следствию, что в растворе нескольких электролитов, которые имеют общими определенные виды ионов, средние коэффициенты активности электролитов зависят друг от друга. [41]
Для растворов с конечной концентрацией уравнение Нернста необходимо модифицировать двояким образом. Во-первых, диффузия определяется градиентом осмотического давления, или химического потенциала ( не обязательно только градиентом концентрации), и поэтому необходимо принимать во внимание средний коэффициент активности электролита. Во-вторых, следует учитывать влияние ионной атмосферы. В отличие от того, что происходит в явлении электропроводности, при диффузии катионы и анионы движутся в одном и том же направлении, и поэтому симметрия ионных атмосфер не нарушается. В этом случае релаксационный эффект отсутствует, но существует небольшой электрофоретический эффект, который для разбавленных растворов был рассчитан Онзагером. Самые точные измерения подтверждают справедливость уравнения Нернста с указанными поправками. [42]
Обратимся теперь к рассмотрению коэффициентов активности мицеллярного раствора - характеристики, тесно связанной с ионной силой. В теориях растворов электролитов в соответствии с формулой (12.12) вводятся коэффициенты активности отдельных ионов f, и, если мицелла трактуется как ион, распространение этого понятия на мицеллы тривиально. На практике же пользуются средними коэффициентами активности электролитов ( как электронейтральных веществ), определяемыми по (6.4) с учетом числа ионов, образующихся при диссоциации одной молекулы вещества. [43]
Метод вычисления коэффициента активности по экспериментальным данным [ см. уравнение (8.7) ] позволяет определить лишь значения средних коэффициентов активности электролита. В настоящее время не существует методов экспериментального определения коэффициентов активности отдельных ионов. При необходимости расчета этих величин обычно принимают, что средний коэффициент активности электролита представляет собой среднее геометрическое коэффициентов активности образующих его ионов. [44]
Приведенный метод позволяет определить лишь значения средних коэффициентов активности электролита. В настоящее время не существует методов экспериментального определения коэффициентов активности отдельных ионов. При необходимости расчета этих величин обычно принимают, что средний коэффициент активности электролита представляет собой среднее геометрическое коэффициентов активности образующих его ионов. [45]
Страницы: 1 2 3 4