Средний коэффициент - активность - электролит
Cтраница 4
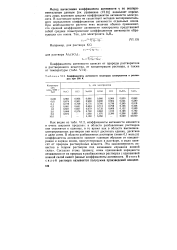 |
Коэффициенты активности некоторых электролитов в растворах при 298 К. [46] |
Метод вычисления коэффициента активности Y по экспериментальным данным [ см. уравнение (VI.8) ] позволяет определить лишь значения средних коэффициентов активности электролита. В настоящее время не существует методов экспериментального определения коэффициентов активности отдельных ионов. При необходимости расчета этих величин обычно принимают, что средний коэффициент активности электролита представляет собой среднее геометрическое коэффициентов активности образующих его ионов. [47]
Согласно этой теории, помимо фиксированных анионов, обеспечивающих неравномерное распределение подвижных ионов различного заряда, аккумуляция ионов калия в клетках должна обеспечиваться еще какими-то специфическими активными группами. Эти активные группы расположены определенным образом в структуре макромолекулы относительно фиксированных анионов и образуют вместе с ними избирательную для ионов калия группировку, сходную по своему характеру с ионными и дипольными комплексами. Образование такого рода комплекса не должно существенным образом влиять на средний коэффициент активности электролита, состоящего из избирательно сорбируемого противоиона и фиксированных ионов. [48]
По смыслу уравнения (6.2), величина рН представляет отрицательный логарифм активности ионов водорода, в свою очередь связанную с концентрацией ионов водорода выражением ац / H CH, в котором / н - коэффициент активности ионов водорода. Если концентрация ионов водорода достаточно мала, можно положить, что коэффициент активности / н будет близок к единице, тогда рН - lgCH - Однако такое приближение утрачивает законность в общем случае. С другой стороны определение коэффициентов активности отдельных ионов является невыполнимой задачей. Существующие методы позволяют найти только средний коэффициент активности электролита в целом. [49]
 |
Схема ионной атмосферы ложного знака. Такая статистическая. [50] |
Поскольку энергия системы с ионной атмосферой имеет электрическую природу, то Дебай и Гюккель предположили, что такая энергия должна быть функцией плотности электрического заряда и потенциала, создаваемых ионной атмосферой. В итоге было получено уравнение, позволяющее рассчитать энергию взаимодействия иона с ионной атмосферой. Затем, используя такое уравнение, Дебай и Гюккель получили уравнение, позволяющее вычислить коэффициент активности иона, а также средний коэффициент активности электролита. Найденное уравнение для коэффициента активности совпадало с уравнением, полученным эмпирически для разбавленных растворов электролитов. [51]
Однако мнение, высказанное Гуггенгеймом [17], о том, что ионный коэффициент активности является не более, чем математической абстракцией, следует рассматривать как преувеличение. Имеются два общих приближения. Первое предполагает элиминирование диффузионного потенциала или его оценку, а второе связано с определением соотношения между той или иной поддающейся измерению комбинацией ионных коэффициентов активности или средних коэффициентов активности электролитов с самими ионными коэффициентами активности. [52]
Страницы: 1 2 3 4