Атом - элемент - группа
Cтраница 1
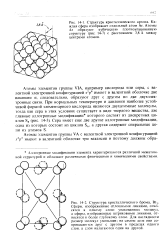
Атомы элементов группы VIA, например кислорода или серы, с валентной электронной конфигурацией s2p4 имеют в валентной оболочке две вакансии и, следовательно, образуют друг с другом по две двухэлек-тронные связи. [2]
Атомы элементов V группы - азота, фосфора и мышьяка - также наблюдались в матричных спектрах ЭПР, которые обнаруживают взаимодействие неспаренного электрона с ядерным спином. Постоянная сверхтонкого взаимодействия для азота сильно зависит от природы матрицы, причем какого-либо усложнения спектра из-за наличия трех неспаренных р-электронов ( 4S состояние) не наблюдается. [3]
Атомы элементов III-IV групп - бор, алюминий, углерод, кремний - образуют с атомами водорода ко-валентные, слабо полярные связи, не склонные к диссоциации. V-VII групп, полярность связи элемент - водород вновь увеличивается, но характер распределения зарядов в возникающем диполе иной, чем для элементов, склонных к потере электронов. Атомы неметаллов, у которых для завершения электронной оболочки необходимо несколько электронов, оттягивают ( поляризуют) к себе пару электронов связи тем сильнее, чем больше заряд ядра. Поэтому в рядах СН4 - NH3 - H2O - HF или SiH4 - PH3 - H2S - HC1 связи атомов водорода, оставаясь ковалентными, приобретают более полярный характер, а атом водорода в диполе связи элемент - водород становится более электроположительным. Если полярные молекулы оказываются в растворе, причем растворитель тоже - полярный, способный вызвать ионизацию ( диссоциацию) связей, то может происходить процесс электролитической диссоциации ( подробно см. гл. [4]
Атомы элементов VIIB группы имеют в d - подуровне по 5 электронов, которые могут принимать участие в химических реакциях наряду с s - электронами наружного уровня. [5]
Атомы элементов VIII группы не имеют непарных электронов и потому образуют с другими простыми веществами ковалентные соединения, которые называют комплексными. [6]
Атомы элементов IVa группы, кроме р-олова и свинца, разделяют четыре валентных электрона со своими четырьмя соседями и образуют решетку типа алмаза с координационным числом, равным четырем. У олова пыше 13 происходит разрушение направленных двухэлектронных связей, внешние электроны становятся свободными, и вследствие этого Р - олово приобретает металлические свойства и ОЦ тетрагональную структуру. У свинца коллективизируются оба 6р - электрона, и ион РЬ2 с двумя 6-электронами имеет внешнюю сферическую оболочку, что приводит к ГЦК структуре. [7]
Атомы элементов группы кислорода имеют шесть электронов во внешней оболочке при застроенных внутренних оболочках. Из шести валентных электронов два вступают в ковалентную связь. [8]
Атомы элементов VI группы характеризуются двумя различными структурами внешнего слоя с наличием в нем либо шести, либо одного или двух электронов. [9]
Атомы элементов группы бора имеют во внешнем слое по 3 электрона. [10]
Атомы элементов группы бора имеют во внешнем слое по в электрона. [11]
Атомы элементов группы бора имеют во внешнем слое по 3 электрона. [12]
Атомы элементов группы бора имеют во внешнем слое по 3 электрона. Валентность 1 проявляется в соединениях алюминия и его аналогов, но наиболее характерна для таллия. [13]
Атомы элементов VI группы характеризуются двумя различными структурами внешнего слоя с наличием в нем либо шести, либо одного или двух электронов. [14]
Атомы элементов группы бора имеют во внешнем елое по 3 электрона. Валентность 1 проявляется в соединениях алюминия и его аналогов, но наиболее характерна для таллия. [15]
Страницы: 1 2 3 4