Атом - элемент - группа
Cтраница 4
Выше указывалось, что атомы элементов IV группы германия и кремния, кристаллизующиеся в решетку типа алмаза, связываются друг с другом гомеополярными связями. Связь такого типа обладает наиболее высокой прочностью. Поэтому в решетке типа алмаза амплитуды тепловых колебаний атома особенно малы. Это, а также и другие обстоятельства обусловливают высокую подвижность носителей тока в германии и кремнии. [46]
Как мы видели, атомы элементов предшествующих групп содержат по одному или соответственно по два валентных электрона. Атомы же элементов III группы имеют по три таких электрона. [47]
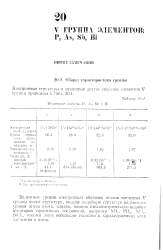 |
Некоторые свойства Р, As, Sb и Bi. [48] |
Валентные уровни электронных оболочек атомов элементов V группы имеют структуру, внешне подобную структуре валентного уровня атома азота, однако, помимо стехиометрического подобия некоторых простейших соединений, например NH: i, PH. [49]
На внешнем электронном уровне атомов элементов I группы находится один электрон ( табл. 16), следовательно, все эти элементы представляют собой металлы. [50]
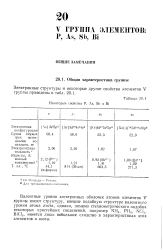 |
Некоторые свойства Р, As, Sb n Bi. [51] |
Валентные уровни электронных оболочек атомов элементов V группы имеют структуру, внешне подобную структуре валентного уровня атома азота, однако, помимо стехиометрического подобия некоторых простейших соединений, например NH3, PH3, NCL, BiCl3, имеется лишь небольшое сходство в характеристиках этих элементов и азота. [52]
Страницы: 1 2 3 4