Атом - элемент - группа
Cтраница 3
 |
Гибридные уровни в атомах бора и углерода. [31] |
У атомов элементов групп IIIA и IVA, которым свойственна максимальная положительная валентность 3 и 4, в основном состоянии содержится только один или два непарных электрона. Максимальная валентность может быть достигнута, если за счет внешней энергии один из электронов пары перейдет на свободную орбиталь в р-подуровне. [32]
В атомах элементов III группы валентные электроны располагаются по электронным слоям неодинаково. [33]
Наконец, атомы элементов группы благородных газов обладают в основном состоянии полностью заполненными оболочками ( так что спин S 0), а их энергии возбуждения велики. [34]
 |
Общая характеристика элементов группы углерода. [35] |
Из строения атомов элементов группы углерода и положения их в периодической системе следует, что они занимают промежуточное место между элементами, атомы которых относительно легко отдают электроны, и элементами, атомы которых присоединяют электроны. [36]
 |
Цепочечные кристаллы. [37] |
Цепочки из атомов элементов VI группы ( в основном селена и теллура) построены таким образом, что их неподеленные электронные пары находятся в наиболее выгодном расположении относительно друг друга. Это достигается винтообразным построением цепочки, которое хорошо видно из рис. 39, а. Повторяемость в этих спиралях наблюдается через каждые три атома. [38]
Присоединение электронов атомами элементов группы кислорода происходит при взаимодействии их с металлами. В соединениях с неметаллами атомы элементов группы кислорода достраивают электронную оболочку до атомов соответствующего инертного газа, путем образования ковалентных связей. [39]
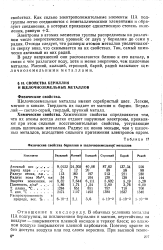 |
Физические свойства бериллия и щелочноземельных металлов. [40] |
Электроны в атомах элементов группы распределены на различном числе энергетических уровней: от двух у бериллия до семи у радия. Отсюда следует, что размеры атомов металлов увеличиваются сверху вниз, что сказывается на их свойствах. Так, самый химически активный из них радий. [41]
 |
Схема фотосъ. [42] |
В отличие от атомов элементов группы меди предпоследний электронный уровень элементов группы цинка является стабильным: из подуровня а10 электроны не отрываются. Валентными электронами являются наружные: максимальное окислительное число элементов равно 2, но только в возбужденном состоянии. [43]
Как уже отмечено, атомы элементов III группы соответственно общему правилу содержат по три валентных электрона. [44]
Как мы видели, атомы элементов предшествующих групп содержат по 1 или соответственно по 2 валентных электрона. Атомы же элементов III группы имеют по 3 таких электрона. [45]
Страницы: 1 2 3 4