Атом - элемент - группа
Cтраница 2
Атомы элементов VI группы характеризуются двумя различными структурами внешнего слоя с наличием в нем либо шести, либо одного или двух электронов. [16]
Атомы элементов VI группы - кислород, сера, селен, теллур внешними 52р4 - электронами, дающие сплетения в расплавленном состоянии, образуют перемычки типа Si-0 - Si между другими атомами ( бор, германий, кремний, мышьяк и др.), что является принципиально важным при стеклообразовании. Атомы элементов шестой группы увязываются ковалентными связями лишь с двумя соседними атомами, входя, таким образом, в сетку в виде звеньев, образующих сплетения часто путем проникновения звеньев одного полиэдра в просвет другого. [17]
Атомы элементов IB группы не вытесняют водород из разбавленных кислот, трудно окисляются, а ионы их легко восстанавливаются до металлов. [18]
Атомы элементов VI группы характеризуются двумя различными структурами внешнего слоя с наличием в нем либо шести, либо одного или двух электронов. [19]
Атомы элементов VIII группы и побочных подгрупп I - VII групп периодической системы элементов имеют во внешнем слое не более двух электронов и в подстилающем слое от 8 до 18 электронов. [20]
Атомы элементов IV группы содержат по 4 валентных электрона. Это ведет к существенному повышению относительной доли неметаллов в числе элементов этой группы. Так С и Si - неметаллы, а остальные проявляют ясно выраженные металлические свойства. [21]
Атомы элементов IV группы содержат по 4 валентных электрона. Это ведет к существенному повышению относительной доли неметаллов в числе элементов этой группы. Так, С и Si - неметаллы, а остальные проявляют ясно выраженные металлические свойства. [22]
Атомы элементов втсрсп группы периодической системы имеют в наружном слое по два электрона Число электронов в более глубоких слоях атомов не у всех элементов одинаково. Этим объясняется деление группы на подгруппы. [23]
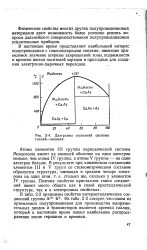 |
Диаграмма состояний системы галлий-мышьяк. [24] |
Атомы элементов III группы периодической системы Менделеева имеют на внешней оболочке на один электрон меньше, чем атомы IV группы, а атомы V группы - на один электрон больше. Поэтому свойства кристаллов таких соединений имеют много общего как в своей кристаллической структуре, так и в электронных свойствах. [25]
Атомам элементов IV группы обычно приписывалось два возможных значения числа валентности - в одних рядах соединений значение, равное двум, в других рядах соединений значение, равное четырем. Следует отметить, что уже давно из экспериментальных данных было ясно, что указанные выше правила, связывающие валентности атомов элементов с группой периодического закона, являются только правилами, но не строгими законами; до настоящего времени эти правила имели исключения. [26]
Атомам элементов группы галогенов недостает по одному электрону, чтобы приобрести строение атомов инертных газов, кроме того, галогены характеризуются большими значениями ПИ. [27]
Вообще атомы элементов V группы, подобно мышьяку, ведут себя в германии ( а также и в кремнии), как простые доноры электронов, отдающие по одному электрону от каждого атома. При наложении внешнего электрического поля эти электроны будут выполнять функцию носителей тока. [28]
Вообще атомы элементов V группы, подобно мышьяку, ведут себя в германии ( а также и в кремнии) как простые доноры электронов, отдающие по одному электрону от каждого атома. При наложении внешнего электрического поля эти электроны будут выполнять функцию носителей тока. [29]
Почему атомы элементов IA группы имеют низкие первые энергии ионизации. [30]
Страницы: 1 2 3 4