Атом - рассматриваемый элемент
Cтраница 2
Находящиеся в нормальном состоянии атомы рассматриваемых элементов содержат во внешней оболочке по пяти электронов, из которых непарными являются три р-электрона. [16]
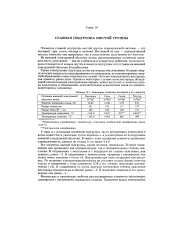 |
Некоторые свойства кислорода и его аналогов. [17] |
Во внешней электронной оболочке атомы рассматриваемых элементов содержат шесть электронов - два на s - орбитали и четыре нар-орбитали. Атом кислорода отличается от атомов других элементов подгруппы отсутствием на внешней электронной оболочке d - подоболочки. [18]
Во внешней электронной оболочке атомы рассматриваемых элементов содержат шесть электронов - два на s - орбитали и четыре на р-орбитали. [19]
Валентность зависит от состояния атомов рассматриваемого элемента, природы партнера, с которым реагирует данный элемент, условий взаимодействия. Так, углерод с одним и тем же партнером - кислородом - в зависимости от условий взаимодействия образует ССЬ и СО, в которых состояния атомов углерода различны. На основе валентности элементов легко определить формульный состав химического соединения. Поэтому величину валентности часто называют стехио-метрической валентностью. [20]
Валентность зависит от состояния атомов рассматриваемого элемента, природы партнера, с которым реагирует данный элемент, условий взаимодействия. Так, углерод с одним и тем же партнером - кислородом - в зависимости от условий взаимодействия образует COj и СО, в которых состояния атомов углерода различны. На основе валентности элементов легко определить формульный состав химического соединения. Поэтому величину валентности часто называют стехио-метрической валентностью. [21]
Заполнение электронами внешних энергетических уровней атомов рассматриваемых элементов, равное половине устойчивого октета ( ns2npe) накладывает особый отпечаток на свойства всей подгруппы. Этим объясняется малое сродство атомов к электрону, в связи с чем элементы: подгруппы углерода не образуют отрицательно заряженных ионов. [22]
Какие степени окисления известны для атомов рассматриваемых элементов. Какие из них наиболее характерны для меди; для серебра; для золота. [23]
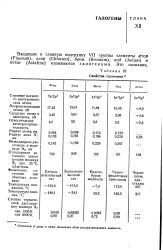 |
Свойства галогенов. [24] |
Символом Э здесь и ниже обозначен атом рассматриваемого элемента. [25]
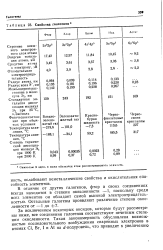 |
Свойства галогенов. [26] |
Символом Э здесь н ниже обозначен атом рассматриваемого элемента. [27]
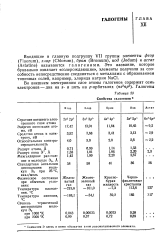 |
Свойства галогенов. [28] |
Символом Э здесь и ниже обозначен атом рассматриваемого элемента. [29]
Символом Э здесь и далее обозначен атом рассматриваемого элемента. [30]
Страницы: 1 2 3 4