Атом - рассматриваемый элемент
Cтраница 3
Как видно, наружный энергетический уровень атомов рассматриваемых элементов в нормальном состоянии одинаков и содержит по два электрона с противоположными спинами. [31]
В таблице X XIV-4 представлено строение атомов рассматриваемых элементов по электронным слоям, а также указаны их атомные массы и плотность. [32]
Смотря по тому, заряжены ли в данном соединении атомы рассматриваемого элемента положительно или отрицательно, различают положительную и отрицательную электрохимические валентности. В элементарном состоянии вещества имеют электрохимическую валентность, равную нулю. [33]
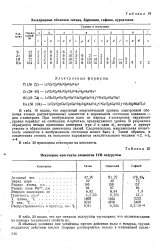 |
Электронные оболочки титана, циркония, гафния, курчатовия. [34] |
В табл. 19 видно, что наружный энергетический уровень электронной оболочки атомов рассматриваемых элементов в нормальном состоянии одинаков - два s - электрона. В результате образуются четыре одиночных электрона ( три d и один s), которые и примут участие в образовании химических связей. [35]
В силу закона равенства действия и противодействия внутренние силы, с которыми действуют друг на друга атомы рассматриваемого элемента объема, в сумме уравновешивают друг друга, и остаются лишь силы, действующие на элемент объема со стороны атомов, расположенных у его поверхности, которые, следовательно, пропорциональны не объему нашего элемента, а площади его поверхности. [36]
 |
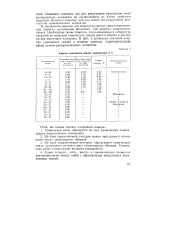
Некоторые свойства элементов подгруппы азота. [37] |
Элементы подгруппы азота могут такж е отдавать электроны, и эта способность выражена у них сильнее, чем у элементов VI и VII групп, что связано с увеличением радиусов атомов рассматриваемых элементов. [38]
К металлам главной подгруппы III группы относятся алюминий, галлий, индий и таллий: Эти элементы являются р-эле-ментами. При возбуждении атомов рассматриваемых элементов один из s - электрояо-в внешнего уровня переходит на р-под-уровень. Поэтому для них характерно трехвалентное: состояние, а для таллия также одновалентное. [39]
Грамм-атом представляет собой массу N атомов рассматриваемого элемента. [40]
Большинство координационных ионов железа и кобальта имеет форму октаэдра. Какой тип гибридизации должен быть наиболее характерным для атомов рассматриваемых элементов. [41]
В побочную подгруппу VII группы периодической системы входят марганец и рений. Интересно, что, несмотря на сходство строения электронной оболочки атомов рассматриваемых элементов и близость их атомных радиусов, каталитические свойства марганца и его соединений резко отличаются от свойств рениевых катализаторов. Так, если для марганцевых контактов характерными являются процессы с участием молекулярного кислорода, то рениевые катализаторы оказались достаточно активными в реакциях гидрирования-дегидрирования. [42]
Впервые понятие о валентности было введено в химию английским химиком Франклендом в 1853 г. Под валентностью, или атомностью, данного элемента он понимал число атомов другого соединяющегося с ним элемента. Если принять валентность водорода равной единице, валентности других элементов определяются как число атомов водорода, соединяющееся с одним атомом рассматриваемого элемента. Франклендом была обнаружена трехва-лентность азота, фосфора, мышьяка и четырехвалентность ( вместе с А. В дальнейшем представления о валентности сыграли исключительно важную роль в теории химического строения Бутлерова и создании Периодической системы химических элементов Менделеева. Это свойство зависит от состояния атомов рассматриваемого элемента, природы партнера, с которым реагирует данный элемент, условий взаимодействия. Так, углерод с одним и тем же партнером - кислородом в зависимости от условий взаимодействия образует С02 и СО, в которых состояния атомов углерода различны. На основе валентности элементов легко определить формульный состав химического соединения. Поэтому величину валентности часто называют стехиометрической валентностью. [43]
Физические и химические свойства Ga, In и Т1 заметно отличаются от свойств А1, несмотря на сходство электронной структуры внешнего энергетического уровня атомов рассматриваемых элементов. [44]
 |
Энергии химических связей, выраженные в эв. [45] |
Страницы: 1 2 3 4