Электрофильный атом
Cтраница 3
Катализатор способствует отрыву протона от гидроксильной группы а-окси-фосфонового эфира. Далее следует нуклеофильная атака отрицательно заряженного кислорода на электрофильный атом фосфора. Этому способствует наличие электроноакцепторных заместителей у карбинольного атома углерода, облегчающих разрыв связи фосфор - углерод. Промежуточный анион е зарядом на углероде присоединяет протон, и образуется продукт перегруппировки. [31]
По поводу строения промежуточного комплекса при электро-фильном замещении в бензоле или его производных на NO2 также не существует определенного мнения. Согласно Титову, комплексо-образование начинается за счет внедрения электрофильного атома нитрующего агента ( в данном случае NOJ) в область л-электронов бензольного ядра. [32]
 |
Схема активного центра фермента карбоксипептидазы ( по данным Липс-комба, Рика, Хартсака, Кешо и Бетджа. [33] |
В результате этих взаимодействий, которые закрепляют в двух точках С-концевой остаток субстрата, пептидная связь в случае, если С-концевая аминокислота представляет собой L-изомер, оказывается направленной на каталитический центр фермента, представленный ионом цинка и оксигруппой тирозина. Поляризация связи СО ионом цинка облегчает нуклеофильную атаку молекулы воды на электрофильный атом С. Участие оксигруппы тирозина обеспечивает синхронное протекание разрыва трех связей и образования трех новых связей в циклическом шестицентровом активированном комплексе. [34]
Притягивающие взаимодействия между группами способны изменять коиформации подвижных гетероциклических систем. Примерами таких взаимодействий могут служить образование водородных связей с гидроксильными группами и трансаннулярные взаимодействия нуклеофильных и электрофильных атомов в средних по размеру циклах. [35]
Имеются данные [10], что аддукт является солью строения I, образующейся при атаке фосфита по электрофильному атому азота. [36]
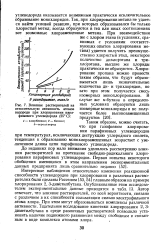 |
Влияние растворителей на относительную активность атомов водорода при хлорировании парафинового углеводорода ( 25 С. 1 - хлорбензол. 2 - бензол. 3-сероуглерод. [37] |
Интересные наблюдения относительно изменения реакционной способности углеводородов при хлорировании в различных растворителях были сделаны Расселом [53, 54] главным образом на примере хлорирования 2, 3-диметилбутана. Автор отмечает, что влияние растворителей, по всей вероятности, связано с различием в их способности сольватации сильно электрофильного атома хлора. При этом могут образовываться комплексы различной активности. [38]
Растворители оказывают огромное влияние на скорость ионных реакций. Под действием растворителей изменяется энергия переходного состояния, они влияют на анионоидный и катионоидный отрыв, а также на агрессивность реагента п ри нуклеофильных и электрофильных атомах. [39]
Механизм реакции Гриньяра с ортоэфирами не был детально изучен. На основании общих знаний о строении и свойствах реагента Гриньяра и ортоэфира наиболее вероятным кажется, что в первую очередь образуется комплекс за счет кислородных атомов ортоэфира и электрофильных атомов магния, который может диссоциировать с образованием диалкоксикарбоний-иона, дающего начало продуктам реакции. Кроме того, диалкоксикарбоний-ион может образоваться при синхронном сдвиге алкоксигруппы, связанной в комплексе, к карбанионной группе из реагента Гриньяра. В реакции могут участвовать в виде недиссоциированных молекул или ионных пар галоалкоксимагнезиаты, алкоксидиалкилмагнезиаты и дигалоалкилмагнезиаты диалкоксикарбония. Возможно, этим объясняется то, что продукты реакции могут возникать по крайней мере двумя путями, из которых один требует более высокой температуры и ( или) более полярных условий. [40]
 |
Относительные константы скорости присоединения. [41] |
В общем для процесса присоединения наличие атомов галогена при С-1 ингибирует радикальную атаку, в то же время галоген при С-2 оказывает активирующее действие. Это видно из сопоставления относительных скоростей реакций ( табл. 3.18); ингибирую-щее действие атома хлора при С-1 может быть связано как с пространственными, так и с полярными эффектами объемистого и электрофильного атома хлора. Однако атом фтора при С-1 ведет себя совершенно по-иному: он не проявляет сколько-нибудь заметного ингибирующего влияния, по крайней мере такого, которое может быть связано с пространственными эффектами, и, как было найдено, теплота полимеризации тетрафторэтилена равна 71 кДж / моль, что даже выше теплоты полимеризации этилена. [42]
Химическая связь, осуществленная электронной парой, перешедшей от одного атома в общее пользование двух атомов, называется донорно-акцеп-торной или координативной. Атом или ион, который отдает неподеленную пару электронов в общее пользование, называется донором или нуклеофильным атомом, а атом, который получает эту электронную пару в общее пользование, называется акцептором или электрофильным атомом. Итак, в образовавшемся ионе аммония четыре связи: три атома водорода, присоединенные к атому азота ковалентной связью, а четвертый - донорно-акцеп-торной. [43]
По мере увеличения электрофильности атомов и ионов переходных металлов возрастает вероятность образования диадсорбированных а-комплексов с участием наиболее основного третичного атома углерода. По-видимому, такие комплексы образуются посредством гетеролитического разрыва углерод-водородной связи. Иными словами, достаточно электрофильный атом металла вытесняет протон и захватывает освободившуюся электронную пару углеродного атома. [44]
По мере увеличения электрофильности атомов и ионов переходных металлов возрастает вероятность образования диадсорбированных а-комплексов с участием наиболее основного третичного атома углерода. По-видимому, такие комплексы образуются посредством гетеролитического разрыва углерод-водородной связи. Иными словами, достаточно электрофильный атом металла вытесняет протон и захватывает освободившуюся электронную пару углеродного атома. [45]
Страницы: 1 2 3 4