Хиральный атом - углерод
Cтраница 2
Абсолютная конфигурация производных миоинозита определяется по низшему хиральному атому углерода. С этой целью формулу изображают соответственно вертикальной проекции Фишера - Толленса так, чтобы С4 располагался наверху. [16]
Если при синтезе образуется молекула с хиральным атомом углерода, то получают смесь энантиомеров ( 1: 1), которые обычно выделяются в виде рацемического соединения. К сожалению, пока известны только немногие примеры таких синтезов, имеющие промышленное применение. Наиболее часто эффект асимметрического синтеза достигается в результате применения оптически активных катализаторов. [17]
Если стадия R-X R - осуществляется при хиральном атоме углерода, почти всегда наблюдается: рацемизация, поскольку свободные радикалы не сохраняют конфигурацию. Исключение составляют циклопропильные субстраты, для которых наблюдалось как обращение [10], так и сохранение [11] конфигурации, а также реакция ( 12), описанная в разд. [18]
Если молекулу растворенного вещества рассматривать вдоль оси, соединяющей хиральный атом углерода и трифторацетилиро-ванный атом азота, то остальные три заместителя располагаются в порядке уменьшения относительных размеров либо по часовой стрелке, либо против нее. Было установлено, что энантиомерам, в которых размеры заместителей уменьшаются по часовой стрелке, соответствует второй пик на хроматограмме, если хроматографиро-вание проводят на фазе 3, полученной из L-валина. Таким образом, для всех алкиловых эфиров N-ТФА-аланина о - энантиомеры элюируются раньше ь-энантиомеров; для метиловых эфиров N-ТФА-лейцина наблюдается обратный порядок, поскольку у них обратные стеричес-кие требования R - и C02R - заместителей. Более того, было зафиксировано понижение степени расщепления в том случае, когда эффективные размеры C02R и R становятся близкими. Наоборот, эффективность расщепления возрастает при увеличении различий в относительных размерах. [19]
Преобразование формул Фишера производят путем четного числа перестановок заместителей у хирального атома углерода. Например, в D-глицериновом альдегиде производят первую перестановку с таким условием, чтобы атом водорода оказался внизу. Для этого меняют его местами с первичноспиртовой группой. Затем определяют направление падения старшинства заместителей. В данном случае оно происходит по часовой стрелке. [20]
Доводы в пользу этого механизма базируются на сохранении конфигурации при хиральном атоме углерода или кремния, а также на наблюдениях ис-присоединения или цис-элиминирования. Эти результаты в высшей степени разумны, поскольку очевидно, что два альтернативных механизма неправдоподобны. Свободнорадикалъные механизмы маловероятны из-за высоких энергий связей и относительно низкого сродства металлов к водороду или углероду. [21]
Диастереофасная дифференциация может также происходить в ненасыщенных соединениях, содержащих не хиральный атом углерода, а хиральный гетероатом. [22]
В органической химии имеется множество соединений, молекулы которых содержат несколько хиральных атомов углерода. При этом, естественно, возрастает число пространственных изомеров одного строения. Если рассматривать взаимосвязи между такими стереоизомерами, то те два, молекулы которых являются зеркальными изображениями друг друга, представляют собой антиподы, а все остальные являются по отношению к ним диастереомерами. Энантиомерия и диастереомерия являются взаимоисключающими типами отношения между двумя стерео-изомерами. Число стереоизомеров с одинаковым строением определяется выражением 2я, где п - число хиральных атомов углерода. [23]
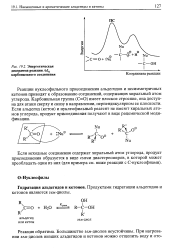 |
Энергетическая диаграмма реакции AdN карбонильного соединения. [24] |
Реакции нуклеофильного присоединения альдегидов и несимметричных кетонов приводят к образованию соединений, содержащих хиральный атом углерода. Карбонильная группа ( СО) имеет плоское строение, она доступна для атаки сверху и снизу в направлении, перпендикулярном ее плоскости. Если альдегид ( кетон) и нуклеофильный реагент не имеют хиральных атомов углерода, продукт присоединения получают в виде рацемической модификации. [25]
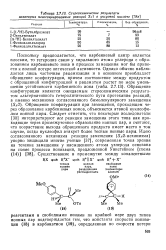 |
Стереохимические результаты некоторых неассоциированных реакций S l в уксусной кислоте [ 38а ]. [26] |
Поскольку предполагается, что карбениевый центр является плоским, то гетеролиз связи у хирального атома углерода с образованием карбениевого иона в процессе замещения мог бы привести к полной потере оптической активности. Обращение конфигурации при замещении, проходящем через образование карбениевых ионов, объясняется атакой нуклеофи-лом ионной пары. Следует отметить, что некоторые исследователи [30] интерпретируют все реакции замещения этого типа как проходящие через промежуточное образование ионных пар, и считают, что возрастание выхода обращенного продукта имеет место в том случае, когда нуклеофил атакует более тесные ионные пары. [27]
Реакции 5д 1 оптически активных спиртов, протекающие с разрывом связи С-ОН у хирального атома углерода, приводят преимущественно к образованию рацемической формы. [28]
 |
А-8. Превращение D-глюкозы в D-арабинозу при помощи деградации по Руффу. [29] |
Здесь везде приведена правильная абсолютная конфигурация Сахаров по Фишеру, но для ясности показаны хиральные атомы углерода. [30]
Страницы: 1 2 3 4