Хиральный атом - углерод
Cтраница 4
В строении моносахаридов заложены возможности существования различных изомеров, так как они содержат хиральные ( асимметрические) атомы углерода. Соединения, отличающиеся расположением заместителей у хирального атома углерода, имеют различные конфигурации и называются конфигурацион-ными изомерами или стереошэмерами. Так, тетрозы имеют два, пенто-зы - три и гексозы - четыре хиральных атома углерода. [46]
Свободные аминокислоты как первичные амины реагируют с HNO2 с отщеплением азота. При этом аминогруппа замещается гидроксилом и изменения конфигурации у хирального атома углерода не происходит. [47]
В молекулах моносахаридов имеются два вида гидроксиль1 - ных групп. Во-первых, это гидроксильная группа, которая свя-зана с хиральным атомом углерода, расположенным по соседству с атомом кислорода в цикле и имеющим наименьший порядковый номер ( атом С ( о в альдозах и атом - С ( 2 в кетозах), и, во-вторых, остальные гидроксильные группы. Первая группа является полуацетальной и обусловливает восстановительные свойства альдоз и кетоз ( восстановление реагентов Фелинга и Толленса, разд. [48]
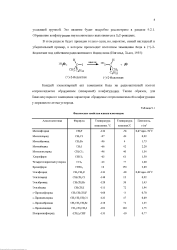 |
Физические свойства алкилгалогенидов. [49] |
Каждый элементарный акт замещения йода на радиоактивный изотоп сопровождается обращением ( инверсией) конфигурации. Таким образом, для бимолекулярного замещения характерно обращение стереохимической конфигурации у хирального атома углерода. [50]
С точки зрения структуры стероиды являются углеводородами или чаще кислородными производными, такими, как - спирты, альдегиды, кетоны и карбоновые кислоты. Стереохимия стероидов очень сложна, поскольку в молекуле циклопен-танопергидрофенантрена имеются шесть хиральных атомов углерода, так что всего существует 64 ( 2е) стереоизомера. Это связано и с тем обстоятельством, что соседние кольца могут быть соединены цис - или гракс-способом ( разд. [51]
Отметим, что из шести атомов углерода молекулы глюкозы четыре атома, с номерами 2, 3, 4 и 5, хиральны, поэтому глюкоза имеет много конфигурационных изомеров. Несколько природных Сахаров отличаются от глюкозы только конфигурацией у одного из четырех хиральных атомов углерода. Эти сахара имеют различные биологические свойства, что еще раз свидетельствует о чрезвычайной специфичности биологических систем. [52]
Для всех аминокислот, за исключением глицина, характерна оптическая активность. Они могут существовать в виде пары энантиомеров - D и L в связи с наличием хирального атома углерода. Протеиногенные аминокислоты существуют только в L-форме, однако в живой природе отмечено наличие D-амино-кислот, находящихся в свободном состоянии или в составе коротких пептидов. [53]
В основу номенклатуры Сахаров положены тривиальные названия моносахаридов состава СлН2йОп с прямой цепью углеродных атомов: ксилоза, рибо-за, глюкоза, фруктоза и др. Наименованиям кетоз придается окончание - улоза, например кетоза С5 - пентулоза. Принадлежность моносахаридов к D - или L-ряду определяется по расположению ОН-группы у последнего ( считая от альдегидной или кетогруп-пы) хирального атома углерода. В качестве стандарта сравнения конфигурации асимметрического атома углерода предложено использовать изомер глицеринового альдегида. [54]
Существует десять гекситов ( табл. 2.3), фишеров-ские проекционные формулы которых изображены на рис. 2.10. Четыре гексита ( 17 - 20) имеют симметрию С2, два ( 21 и 22) - симметрию Cs, а четыре других ( 23 - 26) асимметричны. Приставки ыанно, идо, алло, галакто, глюко, гуло, тало и альтро определяют относительные конфигурации у четырех хиральных атомов углерода. Асимметричные гекситы ( 23 - 26) имеют альтернативные фишеровские проекционные формулы и названия. [55]
Если же изомерное превращение осуществляется в стадии рыхлых ионных пар или свободных ионов, то при использовании меченого растворителя дейтерий присоединяется к карбаниону - процесс изомеризации протекает по межмолекулярному механизму. Таким образом, на основании степени дейтерп-обмена можно делать вывод о том, по какому механизму протекает изомеризация - меж - или внутримолекулярному. Если изомерное соединение имеет хиральный атом углерода при центре реакции и известна величина вращения изомера, то, определяя долю рацемизации, можно иметь дальнейшую информацию о механизме изомеризации. [56]
Для описания структуры кетоз применяются те же правила, что и для альдоз. Здесь следует еще раз напомнить упоминавшееся ранее общее правило ( разд. D - или ь-ряду определяется конфигурацией хирального атома углерода с наибольшим порядковым номером и не имеет отношения к вращению плоскости поляризации света соединением. [57]
 |
Схема синтеза по методу Кори. Хиральный центр показан звез. [58] |
Предшественником а-аминокислоты является соответствующая а-кетокислота. Кетокислота реагирует с хиральным реагентом и образует цикл минимального размера, в который входит гидразон. Специфическое восстановление двойной связи приводит к появлению хирального атома углерода в соответствующей а-аминокислоте. В результате гидрогенолиза этого промежуточного соединения образуются хиральная аминокислота и хиральный вторичный аминоспирт, который можно превратить в исходный хиральный реагент. [59]
Страницы: 1 2 3 4