Периферийный атом
Cтраница 1
При взаимодействии периферийных атомов в состоянии А или Б с адсорбируемыми молекулами происходит обратный переход в нормальное валентное состояние. Поскольку переходы в периферийных атомах требуют затраты определенной энергии, то, вероятно, помол графита при низких температурах должен способствовать сохранению первичного состояния активных центров на поверхности. Сигнал без изменения формы линии сохраняется при повышении температуры до 293 К. Наблюдаемый сигнал ЭПР обусловлен локализованными на 5р2 - орбиталях а-электронами. Интенсивность его близка к интенсивности сигнала неокисленного образца. В данном случае часть хемосорбированного кислорода находится в радикальной форме. [1]
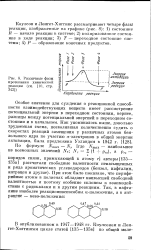 |
Различные фазы протекания химической реакции ( [ 10, стр. 342 ]. [2] |
При этом было показано, что периферийные атомы в полиенах обладают наивысшей свободной валентностью и поэтому особенно склонны к взаимодействию с радикалами и к другим реакциям. Так, в нафталине наиболее реакционноспособны. [3]
 |
Схематическая модель, объясняющая механизм изменения электропроводности углеродистых материалов. [4] |
Атомы углерода в структуре органических веществ связаны с периферийными атомами водорода и кислорода, что обусловливает заполнение нижних энергетических уровней и пустоту верхних. Тепловое движение приводит к перескоку малого числа электронов через барьер и вызывает небольшую проводимость. При 500 - 700 удаляется значительное количество периферийных атомов ( водорода, кислорода, азота) и обнажаются свободные валентности. При этом электроны из я-состояния перескакивают в периферийные орбиты, оставляя в я-уровне пустые полоски ( дыр - - ки), обусловливая этим возможности перескока в них электронов из соседних, занятых состояний, что будет способствовать повышению проводимости. По мере увеличения размеров плоскостей атомов углерода, периферийные ловушки исчезают, так что уровень Ферми в конечном счете, когда образуется совершенный кристалл графита неопределенно больших размеров, возвращается к вершине более низкого уровня. [5]
Как установили Мессмер и др. [732], противоречивые знаки зарядов центрального и периферийных атомов кластеров Wn, Nin ( re 9, 13), полученые в ранних работах одним и тем же методом ЕН, не имеют физического обоснования, но являются следствием различной параметризации. [6]
Эта группа электронов образует одно легковозбудимое электромагнитным полем облако, к-рое в значит, мере экранировано периферийными атомами водорода или радикалами от межмолекулярпых воздействий и мало участвует в кристаллич. [8]
Для комплексов заданного типа значение приобретают такие их характеристики, как устойчивость, заряд, размер, возможность изменения координационного числа, гидрофильность периферийных атомов. [9]
Повышенная плотность положительного заряда обычно приводит к прочной координации воды, увеличению энергии взаимодействия с водой ( а следовательно, и растворимости) и возрастанию ионизации периферийных атомов водорода. Ослабление кислотных свойств у гидросульфат - и гидросульфит-ионов по сравнению с нейтральными кислотами находится в соответствии с отрицательными зарядами этих ионов, которые затрудняют ионизацию протонов, но и в этом случае кислотные свойства серы 6 выражены сильнее. [10]
Галогены имеют значительно больше состояний окисления, чем водород, и гораздо чаще являются центральными атомами в молекулах по сравнению с водородом, который обычно является периферийным атомом. Следует отметить, однако, сходство водорода с фтором в этом отношении. Именно то, что атомы обоих этих элементов обычно находятся на периферии молекул, во многом объясняет, почему химики часто помещают водород в периодической таблице в группу галогенов. [11]
В нашем примере в кластере [ АВ6 ] П центральный атом А, как и в кристалле, окружен шестью ближайшими соседями - атомами типа В, а для периферийных атомов типа В в кристалле АВ, окруженных шестью атомами типа А, геометрия окружения в кластере отличается от таковой для кристалла. [12]
На рис. 15.4 строение каждого из обсуждаемых соединений галогенов рассмотрено с учетом полного числа валентных электронов в молекуле путем отнесения всех валентных электронов к каждому из ее атомов ( по 8 электронов на каждый периферийный атом) и на основании представлений о возможных связывающих орбиталях или гибридизации орбиталей у каждого центрального атома. [13]
Они обнаруживают свойства, свидетельствующие об нх ароматичности. Периферийные атомы лежат не точно в плоскости, максимальное отклонение от средней плоскости равно 0 23 А. [14]
 |
Тетраэдриче-ская структура кристаллической решетки льда. [15] |
Страницы: 1 2 3 4
