Ароматическая аминокислота
Cтраница 3
 |
Спектр флуоресценции дартном растворе 2-нафтиламина. [31] |
Если две различные молекулы расположены достаточно близко, они могут влиять на флуоресценцию друг друга. Такое взаимодействие может происходить между ароматическими аминокислотами, в ферментах и флуоресцирующих коферментах. [32]
Активность аналогов ангиотензина, у которых в положении 4 вместо тирозина содержится остаток фенилаланина, снижена весьма значительно. К тем же результатам приводит и замена ароматической аминокислоты на алифатическую; так, А1а4 - Пеи5 - ангиотензин II ( LIII) обладает лишь 3 % активности Пеи5 - ангиотензина II. Для дез - ( Asp - Arg2) - ангиотензина II ( LXVII), синтезированного Пэйджем и Бампусом [1674], характерно наличие хотя и незначительной ( 1 - 2 %), но достаточно четко выраженной активности; замена в этом соединении остатка тирозина на фенилаланин ( LXIX), аланин ( LXVIII), n - фторфенилаланин ( LXX) или р - 2-тиенил-ь - аланин ( LXXI) приводит к полной потере биологической активности. [33]
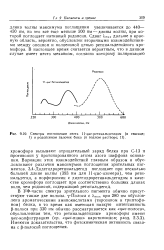 |
Спектры поглощения света И - ис-ретинальдегидом ( в гексане. / и родопсином палочек быка ( в водном растворе. II. [34] |
В УФ-части спектра зрительного пигмента обычно присутствуют также две полосы. Полоса с Ятах при 280 нм обусловлена ароматическими аминокислотами ( тирозином и триптофаном) белка, в то время как имеющая низкую интенсивность р-полоса при 330 нм обычно рассматривается как цис-полоса, обусловленная тем, что ретинальдегидные хромофоры имеют с-конфигурацию ( ср. Имеются доказательства, что фотохимическая активность связана с Р - ПОЛОСОЙ поглощения. [35]
Подробно изучены две карбоксипептидазы - А и В, относящиеся к металлопротеинам и катализирующие отщепление от полипептида С-концевых аминокислот. Карбоксипептидаза А разрывает преимущественно пептидные связи, образованные концевыми ароматическими аминокислотами, а карбоксипептидаза В-связи, в образовании которых участвуют С-концевые лизин и аргинин. [36]
Синтез ароматических аминокислот в грибах не изучался так детально, как синтез ароматических аминокислот в бактериях. Получен [46] мутант Neurospora crassa со сложной потребностью в ароматических аминокислотах, которая снималась добавкой шикимовой кислоты. Получены также мутанты этого гриба [47], которые могут накапливать 5-дегидрошикимовую и префено-вую кислоты. Возможно, что эти ароматические аминокислоты в N. [37]
Одним из путей превращения аминокислот в тканях является распад аминокислот, связанный с отщепление м карбоксильной группы. Ненцкий в 1876 г. выделил из гниющей желатины фенилэтиламин, представляющий продукт декарбоксилирования ароматической аминокислоты - фенилаланина. Впоследствии в результате работ с чистыми бактериальными культурами, воздействуя ими на раствор чистых аминокислот, удалось доказать ферментативную природу реакции и точно охарактеризовать продукты декарбоксилирования. [38]
Одним из путей превращения аминокислот в тканях является распад аминокислот, связанный с отщеплением карбоксильной группы. Ненцкий в 1876 г. выделил из гниющего желатина фенилэтиламин, представляющий продукт декарбоксилирования ароматической аминокислоты - фенилаланина. [39]
Важная особенность пептидил-пептидгидролаз состоит в выборочном ( селективном) характере их действия на пептидные связи в белковой молекуле. Например, пепсин избирательно ускоряет гидролиз пептидных связей, образованных ароматическими или дикарбоновыми аминокислотами, трипсин - связей, образованных аргинином и лизином, химотрипсин - ароматическими аминокислотами. Индивидуальный белок под действием определенного фермента расщепляется на строго определенное количество пептидов. Избирательное действие этих ферментов объясняется тем, что радикал аминокислоты, по соседству с которой гидролизуется пептидная связь, служит для образования фермент-субстратного комплекса. [40]
Для другой области клинических исследований представляет интерес сообщение Зальцера и Балиса [62] об аминокислотах, которые входят в состав дезоксирибонуклеопротеидов ( ДНП) опухолей. Установлено, что ДНП опухолей содержат меньше основных аминокислот, чем ДНП нормальных тканей, и что в некоторых небольших опухолях присутствует также вещество, хроматографически подобное ароматическим аминокислотам. [41]
Если две различные молекулы расположены достаточно близко, они могут влиять на флуоресценцию друг друга. Одна из них, например, может поглощать излучение флуоресценции другой, свидетельствуя о довольно эффективной миграции энергии от одной молекулы к другой при облучении молекулярного комплекса. Такое взаимодействие может происходить между ароматическими аминокислотами, в ферментах и флуоресцирующих коферментах. [42]
Томпсон обнаружила, что фенилаланин и тирозин в этих условиях исчезают полностью даже тогда, когда они не являются С-концевыми аминокислотами. Нежелательное разложение происходит лишь с этими ароматическими аминокислотами независимо от длины цепи. Метод был испытан на примерах постепенного расщепления ДНФ-ди -, ДНФ-три - и ДНФ-тетрапептидов. [43]
В переваривании нативных белков и продуктов их гидролиза в тонком кишечнике активное участие принимают экзопептидазы. Карбоксипептидазы синтезируются в неактивном состоянии в поджелудочной железе и активируются трипсином в кишечнике. Карбоксипептидаза А гидролизует пептидные связи С-концевых аминокислот, образованные преимущественно ароматическими аминокислотами ( фенилаланин, тирозин, триптофан), а карбоксипептидаза В - связи, в образовании которых участвуют С-концевые лизин и аргинин. [44]
Эти ферменты катализируют дальнейший гидролиз белков. Трипсин гидролизует пептидные связи, которые связывают аргинин или лизин с другими кислотами. Химотрипсин гидролизует пептидные связи, в образовании которых принимает участие карбоксильная группа ароматической аминокислоты. Пепсин, трипсин и химо-трипсин катализируют гидролиз пептидных связей, расположенных внутри цепи белка. Такие ферменты называют эндопептидазами. В соке поджелудочной железы содержатся также экзопептидазы, или эрепсины, которые катализируют гидролиз концевых пептидных связей в полипептидах или пептидах. Аминопептидаза гидролизует пептидную связь, образованную концевой кислотой за счет ее карбоксильной группы. Аминогруппа этой кислоты остается свободной. Карбоксипептидаза катализирует гидролиз пептидной связи, в образовании которой участвует аминогруппа концевой 338 кислоты. [45]
Страницы: 1 2 3 4