Корреляционная диаграмма
Cтраница 1
 |
Корреляционная диаграмма для реакции H2 D2 - - 2HD. СТФА ФВ. О ФА-фв. cii, 02 - МО молекул H2 D2, ста и 0р МО молекул HD. [1] |
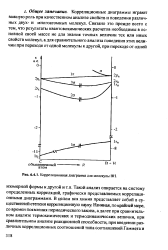
Корреляционная диаграмма такого типа и представлена на рис. 2.7. Если такая корреляционная диаграмма имеет пересекающиеся уровни, то следует ожидать высокой энергии активации реакции. [2]
Корреляционная диаграмма, в которой по оси абсцисс представлен пути реакции, а по оси ординат - уровни энергии, может быть построена путем соединения прямыми линиями орбиталей, соответствующих одной в той же симметрии. [3]
 |
Корреляционная диаграмма для молекулы ВН. [4] |
Корреляционные диаграммы играют важную роль при качественном анализе свойств и поведения различных двух - и многоатомных молекул. [5]
Корреляционная диаграмма для обоих вариантов отнесения показана на рис. 7.3. Помимо спектров п-фторгалогенбензолов, были также интерпретированы спектры п-дихлорбензола, n - дибромбензола, п-ди -: иодбензола и n - бромиодбензола. Отмечено, что симметричное колебание кольца ( а4), по-видимому, наиболее чувстительно к массе заместителя и что самая низкочастотная полоса ( ниже 160 см 1) в спектрах кристаллических соединений при - 170 С на 10 - 20 см 1 выше, чем в спектре жидкости при 20 С. [6]
Корреляционная диаграмма, изображенная на рис. 38, показывает, что высшая занятая орбиталь циклобутана, имеющая симметрию AS, коррелирует с разрыхляющей я Л5 - ор-биталью системы этилен этилен. [7]
Корреляционная диаграмма ( рис. 10.5) имеет одну особенность, которая требует пояснений. При построении корреляционной диаграммы учитывалась весьма общая теорема, касающаяся кривых электронной потенциальной энергии двухатомных молекул и известная как правило непересечения. Согласно этой теореме, потенциальные кривые двухатомной молекулы не могут пересекаться, если соответствующие электронные состояния обладают одинаковой симметрией. [8]
Корреляционная диаграмма для молекулярных орбиталей молекулы НАН в зависимости от угла между связями. [9]
Корреляционные диаграммы позволяют в ряде задач понять в простых терминах особенности электронной структуры молекул и связанные с ней ее геометрические характеристики. Молекула ОН2 изогнута, а молекула MgH2 линейная. Наиболее прямолинейный путь в исследовании геометрических характеристик сводится к вычислению полной энергии как функции угла H-Mg - Н и поиск минимума на соответствующей потенциальной поверхности. В ходе доказательства делают существенное предположение: сумма орбитальных энергий занятых состояний предполагается изменяющейся подобно полной энергии. [10]
 |
Корреляционная диаграмма ИК-спектров кремнеорганических соединений. [11] |
Корреляционная диаграмма дает возможность расшифровывать строение новых кремнеорганических соединений. [12]
 |
Свойства молекулы Li. [13] |
Корреляционные диаграммы могут быть построены и для молекул с большим числом электронов, хотя для них они значительно сложнее. Однако, когда мы строим молекулярные орбитали и с помощью принципа Паули размещаем на них электроны, можно руководствоваться теми же принципами. [14]
Корреляционные диаграммы связывают состояние каждого электрона в объединенном атоме с соответствующими электронными состояниями в изолированных атомах. [15]
Страницы: 1 2 3 4 5