Ароматические аминокислота
Cтраница 3
Помимо трех указанных ароматических аминокислот в ближней ультрафиолетовой области поглощают дисульфидные связи ( рис. и -) - Поскольку характеристики этого процесса зависят от величины двугранных углов, образуемых дисульфидными мостиками, определить вклад данного хромофора в полосу с Хтах 280 нм довольно трудно. [31]
Вопрос о биосинтезе ароматических аминокислот в высших растениях еще более не ясен; это объясняется главным образом отсутствием соответствующих биохимических мутантов и тем, что их трудно получить. Есть причины считать, что путь биосинтеза через шикимовую кислоту все же имеет место и в высших растениях. Так, в растениях широко распространены шикимовая и хинная кислоты, а эксперименты с мечеными атомами показали, что шикимовая кислота может включаться в биосинтез ароматических аминокислот и целого ряда фенольных соединений. На растительном материале были наглядно показаны некоторые ферменты, участвующие в биосинтезе ароматических аминокислот. [32]
Методика ионообменной хроматографии ароматических аминокислот разработана еще очень слабо. [33]
Методика ионообменной хроматографии ароматических аминокислот разработана еще очень слабо. [34]
Первой ступенью в превращении ароматических аминокислот в коричную кислоту и ее производные является ферментативное деза-минирование. Куколь и Конн / 2 О / исследовали прямое превращение фенилаланина в коричную кислоту с помощью ферментов из группы аммонолиаз. [35]
Метод основан на способности ароматических аминокислот ( триптофана, тирозина и в меньшей степени фенилаланина) поглощать ультрафиолетовый свет с максимумом при 280 нм. Измеряя величину оптической плотности при этой длине волны, находят количество белка в растворе. Поскольку белки отличаются по содержанию ароматических аминокислот, их поглощение в ультрафиолетовой области спектра может сильно различаться. [36]
Число описанных аномалий обмена ароматических аминокислот довольно значительно; между тем о подобных нарушениях в обмене аминокислот жирного ряда известно немного. [37]
Ниже приведены RJ некоторых ароматических аминокислот для трех систем растворителей. [38]
Примером поверхностноактивных сложных эфиров ароматических аминокислот являются цетил-л-аминобензоат или додецилантранилат. [39]
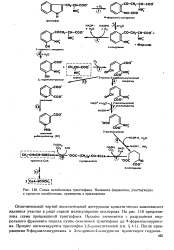 |
Схема катаболизма триптофана. Названия ферментов, участвующих в процессе катаболизма, приведены в приложении. [40] |
Отличительной чертой окислительной деструкции ароматических аминокислот является участие в ряде стадий молекулярного кислорода. На рис. 118 представлена схема превращений триптофана. Процесс начинается с разрушения пир-рольного фрагмента индола путем окисления триптофана до N-формилкинурени-на. [41]
В природе играют существенную роль ароматические аминокислоты, содержащие амино - и карбоксильную группу в боковой цепи. [42]
В природе играют существенную роль ароматические аминокислоты, содержащие амино - и карбоксильную группу в боковой цепи. Две аминокислоты являются продуктами гидролиза белковых веществ. [43]
В природе играют существенную роль ароматические аминокислоты, содержащие амино - и карбоксильную группу в боковой цепи. [44]
Высшие животные не могут синтезировать ароматические аминокислоты de novo, однако показано, что в организме животных возможны некоторые реакции ароматизации циклических соединений. [45]
Страницы: 1 2 3 4